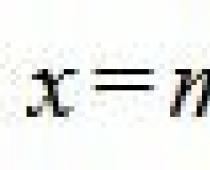Окислительно-восстановительные ферменты, катализирующие перенос электронов, и окислительное фосфорилирование локализованы в липидном слое внутренней мембраны митохондрий клеток.
Транспорт электронов к кислороду в митохондриях (рис. 13.3) происходит в несколько этапов и представляет собой цепь из переносчиков электронов, у которых по мере приближения к кислороду возрастает редокс-потенциал (соответственно снижается восстановительный потенциал). Эти транспортные системы получили название дыхательных цепей.
Рис. 13.3.
Большинство электронных пар поступает в дыхательную цепь благодаря действию ферментов (дегидрогеназ), использующих в качестве акцепторов электронов коферменты NAD+ и NADP + . Всю эту группу ферментов называют ЫАО(Р)-зависимыми дегидрогеназами.
Коферменты NAD + (никотинамид-адениндинуклеотид), FAD и FMN (флавинадениндинуклеотид и флавинмононуклеотид), ко- фермент Q (CoQ), семейство гемсодержащих белков - цитохромов (обозначаемых как цитохромы b, Q, С, А, А 3) и белки, содержащие негеминовое железо, являются промежуточными переносчиками в дыхательной цепи у высших организмов. Процесс начинается с переноса протонов и электронов от окисляемого субстрата на коферменты NAD+ или FAD и образования NADH и FADH2.
Последующее движение электронов от NADH и FADH 2 к кислороду можно уподобить скатыванию с лестницы, ступеньками которой являются переносчики электронов. При каждом шаге со ступеньки на ступеньку высвобождается порция свободной энергии (см. рис. 13.3).
В переносе электронов от органических субстратов к молекулярному кислороду принимают участие три белковых комплекса (I, III, IV) и две подвижные молекулы-переносчики: убихинон (ко- фермент Q) и цитохром С.

Рис. 13.4. Строение молекулы гема, z = 2* или 3 +
Сукцинатдегидрогеназа, принадлежащая собственно к циклу Кребса, также может рассматриваться как комплекс II дыхательной цепи.
Комплексы дыхательной цепи построены из множества полипептидов и содержат ряд различных окислительно-восстановительных кофер- ментов, связанных с белками.
Переносчики электронов цито- хромы (названные так из-за своей окраски) - это белки, содержащие в качестве простетической группы различные группы гемов. Гемы типа Ь соответствуют гемоглобинам. Гем ковалентно связан с белком (рис. 13.4).
Общим для цитохромов является способность иона железа, находящегося в геме, изменять степень окисления при передаче электрона:

Флавинзависимые дегидрогеназы - это белки, у которых сульфгидрильные группы цистеина, входящего в состав белка, связаны с атомами железа, в результате чего образуется железосерные комплексы (центры). Как и в цитохромах, атомы железа в таких центрах способны отдавать и принимать электроны, переходя поочередно в ферри- (Fe +3) и ферро- (Fe +2) состояния.
Железосерные центры функционируют совместно с флавинсодержащими ферментами FAD или FMN.
Фпавинадениндинуклеотид (FAD) является производным витамина В 2 (рибофлавина). Восстанавливаясь, FAD (окисленная форма) присоединяет два атома водорода и превращается в FADH 2 (восстановленная форма):

Еще один переносчик электронов, относящийся к данной группе, - флавинмононуклеотид (FMN) также является производным витамина В 2 (отличается от витамина В 2 только наличием фосфатной группы).
Оба флавиновых кофермента могут существовать и в форме так называемых семихинонов - свободных радикалов, которые образуются в результате переноса только одного электрона на FAD или FMN:

Общее обозначение различных флавопротеидов, различающихся белковой составляющей фермента, - FP„.
Пиридинзависимые дегидрогеназы получили такое название потому, что коферментом для них служат NAD + и NADP + , в молекулах которых имеется производное пиридина - никотинамид:

Катализируемые этими ферментами реакции можно представить следующим образом:

Дегидрогеназы, связанные с NAD + , принимают участие главным образом в процессе дыхания, т.е. в процессе переноса электронов от субстратов к кислороду, тогда как дегидрогеназы, связанные с NADP + , участвуют преимущественно в переносе электронов от субстратов, возникающих в результате катаболиче- ских реакций, к восстановительным реакциям биосинтеза.
Единственный небелковый переносчик электронов - убихинон, названный так потому, что этот хинон встречается везде (от ubiquitous - вездесущий). Сокращенно его обозначают CoQ или просто Q. Убихинон при восстановлении присоединяет не только электроны, но и протоны. При одноэлектронном переносе он превращается в семихинон, двухэлектронном - в гидрохинон.
Последовательность переносчиков электронов в дыхательной цепи митохондрий можно представить следующей схемой:

Эта схема описывается цепью последовательных реакций:


Таким путем через дыхательную цепь электроны от субстратов достигают конечного акцептора - атмосферного кислорода. Образующаяся в результате этого процесса вода называется метаболической.
Разделение водорода на протоны и электроны в мембране митохондрий представляет собой цепь переноса электронов, которая работает как протонный насос, перекачивающий ионы водорода из межклеточного пространства на наружную сторону мембраны.
ЭТЦ локализована в ЦПМ , у эукариот - на внутренней мембране митохондрий . Переносчики расположены по своему окислительно-восстановительному потенциалу , транспорт электрона на всём протяжении цепи протекает самопроизвольно.
Протонный потенциал преобразуется АТФ-синтазой в энергию химических связей АТФ . Сопряжённая работа ЭТЦ и АТФ-синтазы носит название окислительного фосфорилирования .
Цепь переноса электронов митохондрий
Влияние окислительного потенциала
| Восстановитель | Окислитель | Ео´, В |
|---|---|---|
| Н2 | 2 + | - 0,42 |
| НАД Н + Н+ | НАД + | - 0,32 |
| НАДФ Н + Н+ | НАДФ + | - 0,32 |
| Флавопротеин (восстановл.) | Флавопротеин (окисл.) | - 0,12 |
| Кофермент Q Н2 | Кофермент Q | + 0,04 |
| Цитохром B (Fe2+) | Цитохром B (Fe3+) | + 0,07 |
| Цитохром C 1 (Fe2+) | Цитохром C 1 (Fe3+) | + 0,23 |
| Цитохромы A (Fe2+) | Цитохромы A(Fe3+) | + 0,29 |
| Цитохромы A3 (Fe2+) | Цитохромы A3 (Fe3+) | +0,55 |
| H2O | ½ О2 | + 0,82 |
Ингибиторы дыхательной цепи
Некоторые вещества блокируют перенос электронов через комплексы I, II, III, IV .
- Ингибиторы I комплекса - барбитураты , ротенон , пиерицидин
- Ингибитор II комплекса - малонат .
- Ингибитор III комплекса - антимицин А , миксотиазол , стигматтелин
- Ингибиторы IV комплекса - сероводород , цианиды , угарный газ , оксид азота, азид натрия
Электронтранспортные цепи бактерий
Бактерии, в отличие от митохондрий, используют большой набор доноров и акцепторов электронов, а также разные пути переноса электрона между ними. Эти пути могут осуществляться одновременно, например, E. coli при выращивании на среде, содержащей глюкозу в качестве основного источника органического вещества, использует две НАДН дегидрогеназы и две хинолоксидазы, что означает наличие 4 путей транспорта электрона. Большинство ферментов ЭТЦ индуцибельны и синтезируются только в случае, если путь, в который они входят, востребован.
Донором электрона помимо органического вещества у бактерий могут выступать молекулярный водород , угарный газ , аммоний , нитрит , сера , сульфид , двухвалентное железо . Вместо НАДН и сукцинатдегидрогеназы могут присутствовать формиат -, лактат -, глицеральдегид-3-фосфатдегидрогеназа, гидрогеназа и т. д. Вместо оксидазы, использующейся в аэробных условиях, в отсутствие кислорода бактерии могут использовать редуктазы, восстанавливающие различные конечные акцепторы электрона: фумаратредуктазу , нитрат- и нитритредуктазу и т. д.
См. также
Напишите отзыв о статье "Дыхательная цепь переноса электронов"
Примечания
Отрывок, характеризующий Дыхательная цепь переноса электронов
– Ваше благородие, к генералу. Здесь в избе стоят, – сказал фейерверкер, подходя к Тушину.– Сейчас, голубчик.
Тушин встал и, застегивая шинель и оправляясь, отошел от костра…
Недалеко от костра артиллеристов, в приготовленной для него избе, сидел князь Багратион за обедом, разговаривая с некоторыми начальниками частей, собравшимися у него. Тут был старичок с полузакрытыми глазами, жадно обгладывавший баранью кость, и двадцатидвухлетний безупречный генерал, раскрасневшийся от рюмки водки и обеда, и штаб офицер с именным перстнем, и Жерков, беспокойно оглядывавший всех, и князь Андрей, бледный, с поджатыми губами и лихорадочно блестящими глазами.
В избе стояло прислоненное в углу взятое французское знамя, и аудитор с наивным лицом щупал ткань знамени и, недоумевая, покачивал головой, может быть оттого, что его и в самом деле интересовал вид знамени, а может быть, и оттого, что ему тяжело было голодному смотреть на обед, за которым ему не достало прибора. В соседней избе находился взятый в плен драгунами французский полковник. Около него толпились, рассматривая его, наши офицеры. Князь Багратион благодарил отдельных начальников и расспрашивал о подробностях дела и о потерях. Полковой командир, представлявшийся под Браунау, докладывал князю, что, как только началось дело, он отступил из леса, собрал дроворубов и, пропустив их мимо себя, с двумя баталионами ударил в штыки и опрокинул французов.
– Как я увидал, ваше сиятельство, что первый батальон расстроен, я стал на дороге и думаю: «пропущу этих и встречу батальным огнем»; так и сделал.
Полковому командиру так хотелось сделать это, так он жалел, что не успел этого сделать, что ему казалось, что всё это точно было. Даже, может быть, и в самом деле было? Разве можно было разобрать в этой путанице, что было и чего не было?
– Причем должен заметить, ваше сиятельство, – продолжал он, вспоминая о разговоре Долохова с Кутузовым и о последнем свидании своем с разжалованным, – что рядовой, разжалованный Долохов, на моих глазах взял в плен французского офицера и особенно отличился.
– Здесь то я видел, ваше сиятельство, атаку павлоградцев, – беспокойно оглядываясь, вмешался Жерков, который вовсе не видал в этот день гусар, а только слышал о них от пехотного офицера. – Смяли два каре, ваше сиятельство.
На слова Жеркова некоторые улыбнулись, как и всегда ожидая от него шутки; но, заметив, что то, что он говорил, клонилось тоже к славе нашего оружия и нынешнего дня, приняли серьезное выражение, хотя многие очень хорошо знали, что то, что говорил Жерков, была ложь, ни на чем не основанная. Князь Багратион обратился к старичку полковнику.
– Благодарю всех, господа, все части действовали геройски: пехота, кавалерия и артиллерия. Каким образом в центре оставлены два орудия? – спросил он, ища кого то глазами. (Князь Багратион не спрашивал про орудия левого фланга; он знал уже, что там в самом начале дела были брошены все пушки.) – Я вас, кажется, просил, – обратился он к дежурному штаб офицеру.
– Одно было подбито, – отвечал дежурный штаб офицер, – а другое, я не могу понять; я сам там всё время был и распоряжался и только что отъехал… Жарко было, правда, – прибавил он скромно.
Кто то сказал, что капитан Тушин стоит здесь у самой деревни, и что за ним уже послано.
– Да вот вы были, – сказал князь Багратион, обращаясь к князю Андрею.
– Как же, мы вместе немного не съехались, – сказал дежурный штаб офицер, приятно улыбаясь Болконскому.
– Я не имел удовольствия вас видеть, – холодно и отрывисто сказал князь Андрей.
Все молчали. На пороге показался Тушин, робко пробиравшийся из за спин генералов. Обходя генералов в тесной избе, сконфуженный, как и всегда, при виде начальства, Тушин не рассмотрел древка знамени и спотыкнулся на него. Несколько голосов засмеялось.
– Каким образом орудие оставлено? – спросил Багратион, нахмурившись не столько на капитана, сколько на смеявшихся, в числе которых громче всех слышался голос Жеркова.
Тушину теперь только, при виде грозного начальства, во всем ужасе представилась его вина и позор в том, что он, оставшись жив, потерял два орудия. Он так был взволнован, что до сей минуты не успел подумать об этом. Смех офицеров еще больше сбил его с толку. Он стоял перед Багратионом с дрожащею нижнею челюстью и едва проговорил:
– Не знаю… ваше сиятельство… людей не было, ваше сиятельство.
– Вы бы могли из прикрытия взять!
Что прикрытия не было, этого не сказал Тушин, хотя это была сущая правда. Он боялся подвести этим другого начальника и молча, остановившимися глазами, смотрел прямо в лицо Багратиону, как смотрит сбившийся ученик в глаза экзаменатору.
Молчание было довольно продолжительно. Князь Багратион, видимо, не желая быть строгим, не находился, что сказать; остальные не смели вмешаться в разговор. Князь Андрей исподлобья смотрел на Тушина, и пальцы его рук нервически двигались.
– Ваше сиятельство, – прервал князь Андрей молчание своим резким голосом, – вы меня изволили послать к батарее капитана Тушина. Я был там и нашел две трети людей и лошадей перебитыми, два орудия исковерканными, и прикрытия никакого.
Князь Багратион и Тушин одинаково упорно смотрели теперь на сдержанно и взволнованно говорившего Болконского.
– И ежели, ваше сиятельство, позволите мне высказать свое мнение, – продолжал он, – то успехом дня мы обязаны более всего действию этой батареи и геройской стойкости капитана Тушина с его ротой, – сказал князь Андрей и, не ожидая ответа, тотчас же встал и отошел от стола.
В короткой дыхательной цепи окисляется субстрат, для которых первичным акцептором электронов является флапротеид (отсутствует этап окисления субстрата НАД-ДГ). Вещества короткой цепи: янтарная кислота, активные формы жирных кислот, глицерофосфат).
Первая реакция окисления:
В последующем ФАДН 2 при участии (FeS*) + КоQ, окисляется:
Восстановленный КоQ как и в длиной дыхательной цепи системой цитохромов:

Эти дыхательные цепи могут быть разделены на структурно-функциональные форагменты, которые называются окислительные комплексы. В длинной цепи выделяют 3 комплекса, а в короткой 2.
1. Располагается между НАДН 2 и КоQ и включает в себя ФП и FeS комплекс.
2. КоQН 2 -ДГ (цитохром С-редуктазный комплекс) располагается между КоQ и цС и включает в себя цВ, FeS, белки, цС 1
3. Цитохромоксидазный комплекс – окисляет цС и включает в себя цаа 3
4. Сукцинатдегидрогеназный комплекс включает ФП* и FeS, сукцинатДГ
Каждый дыхательный комплекс может быть выключен из работы дыхательной цепи определенными веществами – ингибиторами.
Первый комплекс – амитал, барбитураты, ротенол
Второй комплекс – малонат
Третий комплекс – антимицин А
Четвертый комплекс – Н 2 S, цианиды, СО
Внутримитохондриальное окисление тесно связано с энергетическим обменом. Энергетический обмен – сбалансированность протекания реакций образования и реакций использования энергии.
Реакции идущие с высвобождением энергии называется экзоргиническими реакциями с поглощением эндорганическими. Основным экзорганическим процессом в организме является транспорт электронов по дыхательной цепи. Начальные компоненты НАД окисленный, НАД восстановленный:
 Поэтому в ЦПЭ происходит перемещение электронов с большой энергией, в процессе транспорта электронов энергия высвобождается. Та энергия которая может быть использована на выполнение какой-то работы – свободная энергия
. В дыхательной цепи энергия рассчитывается.
Поэтому в ЦПЭ происходит перемещение электронов с большой энергией, в процессе транспорта электронов энергия высвобождается. Та энергия которая может быть использована на выполнение какой-то работы – свободная энергия
. В дыхательной цепи энергия рассчитывается.
ΔF = -23*n*Δе ,
где n- количество переносимых электронов на атом О 2 (2е), Δе – перепад ОВП между началом и концом ЦПЭ.
Δе = 0,82 –(-0,32)=1,14В
ΔF = -23*2*1,14 = -52 ккал/моль
Эта энергия может быть использована организмом на выполнение различных процессов:
- Механических – сокращение мышц
- Химических – на синтез новых веществ
- Осмотических – перенос ионов против градиента концентрации
- Электрических – возникновение потенциалов в нервной системе
Все организмы в зависимости от энергии, которую они используют делят на два вида: фототрофы – могут использовать энергию солнечного света, хемовары – могут использовать энергию только химических связей особых макроэргических веществ.
Макроэргические вещества – вещества при гидролизе связей которых высвобождается энергия более 5 ккал/моль. К ним относят фосфоенолпируват, креатинфосфат, 1,3-дифосфоглицеринфосфат, ацилы жирных кислот, АТФ (ГТФ, ЦТФ, УЦФ). Среди перечисленных макроэргов центральное место занимает АТФ. АТФ является аккумулятором и источником химической энергии. В молекулярном АТФ заключена энергия на 7,3 ккал/моль (в стандартных условиях) и до 12 ккал/моль в физиологических условиях. Состав АТФ: аденил-рибоза-Н 3 РО 4 - Н 3 РО 4 -Н 3 РО 4 . Синтезируется АТФ из АДФ. Распад АТФ является экзоорганическим процессом. Основным источником энергии для синтеза АТФ является перенос электронов по дыхательной цепи. Присоединение Н 3 РО 4 называется – фосфолирироваием.
Окислительное фосфолирирование
Процесс синтеза АТФ из АДФ и Н 3 РО 4 , за счет энергии транспорта по ЦПЭ. Процессы окисления дыхательной цепи и синтеза АТФ тесно сопряжены. При этом ведущим процессом является транспорт электронов, сопутствующим является фосфолирирование. Участки дыхательной цепи на которых происходит синтез АТФ называются участками сопряжения. Их в длинной цепи три (1, 3, 4 – окислительные комплексы), в короткой дыхательной цепи их два (3,4). Если вещество окисляется в дыхательной цепи, то максимум синтезируются три молекулы АТФ. Эффективность сопряжения окислительного фосфолирирования выражается коэффициентом фосфолирирования. Он показывает сколько молекул Н 3 РО 4 присоединяется к АДФ при переносе двух электронов на один атом кислорода то есть сколько синтезируется молекул АТФ на один атом кислорода. Для длинной цепи коэффициент = 3 для короткой 2.
Механизм окислительного фосфолирирования.
Впервые в тридцатые годы акт синтеза АТФ в процессе окисления был выявлен отечественным биохимиком Энгельгардтом. Основной гипотезой объяснения механизма окислительного фосфолирирования стала хемоосмотическая  теория Митчелла. Согласно ей при транспорте электронов по дыхательной цепи возникает протонный потенциал, который и аккумулирует освободившийся при переносе электрона энергию. В последствии протонный потенциал используется для синтеза АТФ. Возникновение протонного потенциала связано непроницаемость для протонов внутренней мембраны митохондрий. В результате транспорта электронов по дыхательной цепи одновременно происходит выталкивание Н + из матрикса в межмембранное пространство. Переносится 6 – 10 Н+.
теория Митчелла. Согласно ей при транспорте электронов по дыхательной цепи возникает протонный потенциал, который и аккумулирует освободившийся при переносе электрона энергию. В последствии протонный потенциал используется для синтеза АТФ. Возникновение протонного потенциала связано непроницаемость для протонов внутренней мембраны митохондрий. В результате транспорта электронов по дыхательной цепи одновременно происходит выталкивание Н + из матрикса в межмембранное пространство. Переносится 6 – 10 Н+.
Дыхательная цепь является частью процесса окислительного фосфорилирования . Компоненты дыхательной цепи катализируют перенос электронов от НАДН + Н + или восстановленного убихинона (QH 2) на молекулярный кислород. Из-за большой разности окислительно-восстановительных потенциалов донора (НАДН + Н + и, соответственно, QH 2) и акцептора (О 2) реакция является высокоэкзергонической . Большая часть выделяющейся при этом энергии используется для создания градиента протонов и, наконец, для образования АТФ с помощью АТФ-синтазы.
Компоненты дыхательной цепи
Дыхательная цепь включает три белковых комплекса (комплексы I, III и IV ), встроенных во внутреннюю митохондриальную мембрану, и две подвижные молекулы-переносчики - убихинон (кофермент Q) и цитохром с. Сукцинатдегидрогеназа , принадлежащая собственно к цитратному циклу, также может рассматриваться как комплекс II дыхательной цепи. АТФ-синтаза иногда называется комплексом V , хотя она не принимает участия в переносе электронов.
Комплексы дыхательной цепи построены из множества полипептидов и содержат ряд различных окислительно-восстановительных коферментов , связанных с белкам. К ним принадлежат флавин [ФМН (FMN) или ФАД (FAD), в комплексах I и II], железо-серные центры (в I, II и III) и группы гема (в II, III и IV). Детальная структура большинства комплексов еще не установлена.
Электроны поступают в дыхательную цепь различными путями. При окислении НАДН + Н + комплекс I переносит электроны через ФМН и Fe/S-центры на убихинон. Образующиеся при окислении сукцината, ацил-КоА и других субстратов электроны переносятся на убихинон комплексом II или другой митохондриальной дегидрогеназой через связанный с ферментом ФАДН 2 или флавопротеин. При этом окисленная форма кофермента Q восстанавливается в ароматический убигидрохинон . Последний переносит электроны в комплекс III , который поставляет их через два гема b, один Fe/S-центр и гем с 1 на небольшой гемсодержащий белок цитохром с . Последний переносит электроны к комплексу IV, цитохром с-оксидазе. Цитохром с-оксидаза содержит для осуществления окислительно-восстановительных реакций два медьсодержащих центра (Cu A и Cu B) и гемы а и а 3 , через которые электроны, наконец, поступают к кислороду . При восстановлении О 2 образуется сильный основной анион О 2- , который связывает два протона и переходит в воду. Поток электронов сопряжен с образованным комплексами I, III и IV протонным градиентом .
Организация дыхательной цепи
Перенос протонов комплексами I, III и IV протекает векторно из матрикса в межмембранное пространство. При переносе электронов в дыхательной цепи повышается концентрация ионов H + , т. е. понижается значение рН. В интактных митохондриях по существу только АТФ-синтаза позволяет осуществить обратное движение протонов в матрикс. На этом основано важное в регуляторном отношении сопряжение электронного переноса с образованием АТФ.
Как уже упоминалось, все комплексы с I по V интегрированы во внутренней мембране митохондрий, тем не менее обычно они не контактируют друг с другом, так как электроны переносятся убихиноном и цитохромом с. Убихинон благодаря неполярной боковой цепи свободно перемещается в мембране. Водорастворимый цитохром с находится на внешней стороне внутренней мембраны.
Окисление НАДН (NADH) комплексом I происходит на внутренней стороне мембраны, а также в матриксе, где происходит также цитратный цикл и β-окисление - самые важные источники НАДН. В матриксе протекают, кроме того, восстановление O 2 и образование АТФ (ATP). Полученный АТФ переносится по механизму антипорта (против АДФ) в межмембранное пространство, откуда через порины проникает в цитоплазму.
Всего цепь переноса электронов (англ. electron transport chain ) включает в себя разнообразные белки, которые организованы в 4 больших мембраносвязанных мульферментных комплекса. Также существует еще один комплекс, участвующий не в переносе электронов, а синтезирующий АТФ.
Строение ферментативных комплексов
дыхательной цепи
1 комплекс. НАДН-КоQ-оксидоредуктаза
Этот комплекс также имеет рабочее название НАДН-дегидрогеназа , содержит ФМН, 42 белковых молекулы, из них не менее 6 железосерных белков.
Функция
- Принимает электроны от НАДН и передает их на коэнзим Q (убихинон).
Железосерные белки (FeS-белки) – это белки содержащие атомы железа, которые соединены с атомами серы и с серой остатков цистеина. В результате образуется железо-серный центр.

2 комплекс. ФАД-зависимые дегидрогеназы
Данный комплекс как таковой не существует, его выделение условно. К нему относятся ФАД-зависимые ферменты , расположенные на внутренней мембране – например, ацил-SКоА-дегидрогеназа (β-окисление жирных кислот), сукцинатдегидрогеназа (цикл трикарбоновых кислот), митохондриальная глицерол-3-фосфат-дегидрогеназа (челночный механизм переноса атомов водорода).
Функция
- Восстановление ФАД в окислительно-восстановительных реакциях.
- Обеспечение передачи электронов от ФАДН 2 на железосерные белки внутренней мембраны митохондрий. Далее эти электроны попадают на коэнзим Q (убихинон ).
3 комплекс. КоQ-цитохром c -оксидоредуктаза
По другому данный комплекс называется цитохром с редуктаза. В его составе имеются молекулы цитохрома b и цитохрома c 1 , железо-серные белки. Комплекс представляет собой 2 мономера, в каждом из которых насчитывается 11 полипептидных цепей.
Функция
- Принимает электроны от коэнзима Q и передает их на цитохром с .
- Переносит 2 иона Н + на наружную поверхность внутренней митохондриальной мембраны.
Имеются разногласия по поводу количества переносимых ионов H + при участии 3-го и 4-го комплексов. По одним данным, третий комплекс переносит 2 иона H + и четвертый комплекс переносит 4 иона H + . По другим авторам, наоборот, третий комплекс переносит 4 иона H+ и четвертый комплекс переносит 2 иона H+ .
4 комплекс. Цитохром с-кислород-оксидоредуктаза
В этом комплексе находятся цитохромы а и а 3 , он называется также цитохромоксидаза , состоит из 13 субъединиц. В комплексе имеются ионы меди , соединенные с белками комплекса через HS-группы цистеина, и формирующие центры, подобные тем, что имеются в железо-серных белках.
Функция
- Принимает электроны от цитохрома с и передает их на кислород с образованием воды.
- Переносит 4 иона Н + на наружную поверхность внутренней митохондриальной мембраны.
5 комплекс
Пятый комплекс – это фермент АТФ-синтаза , состоящий из множества белковых цепей, подразделенных на две большие группы:
- одна группа формирует субъединицу F o (произносится со звуком "о", а не "ноль" т.к олигомицин-чувствительная) – ее функция каналообразующая , по ней выкачанные наружу протоны водорода устремляются в матрикс.
- другая группа образует субъединицу F 1 – ее функция каталитическая , именно она, используя энергию протонов, синтезирует АТФ.
Механизм работы АТФ-синтазы получил название