ΟΡΙΣΜΟΣ
Νικέλιο- εικοστό όγδοο στοιχείο Περιοδικός Πίνακας. Ονομασία - Ni από το λατινικό "niccolum". Βρίσκεται στην τέταρτη περίοδο, VIIB ομάδα. Αναφέρεται σε μέταλλα. Το πυρηνικό φορτίο είναι 28.
Όπως το κοβάλτιο, το νικέλιο εμφανίζεται στη φύση κυρίως με τη μορφή ενώσεων με αρσενικό ή θείο. τέτοια, για παράδειγμα, είναι τα ορυκτά kupfernickel NiAs, η λάμψη αρσενικού-νικελίου NiAsS, κ.λπ. Το νικέλιο είναι πιο κοινό από το κοβάλτιο [περίπου 0,01% (β.) του φλοιού της γης].
Το μέταλλο νικελίου έχει ασημί χρώμα με κιτρινωπή απόχρωση (Εικ. 1), είναι πολύ σκληρό, γυαλίζει καλά και έλκεται από έναν μαγνήτη. Χαρακτηρίζεται από υψηλή αντοχή στη διάβρωση - σταθερό στην ατμόσφαιρα, στο νερό, στα αλκάλια και σε μια σειρά από οξέα. Διαλύεται ενεργά νιτρικό οξύ. Η χημική αντίσταση του νικελίου οφείλεται στην τάση του για παθητικοποίηση - στο σχηματισμό μεμβρανών οξειδίου στην επιφάνεια που έχουν ισχυρή προστατευτική δράση.
Ρύζι. 1. Νικέλιο. Εμφάνιση.
Ατομική και μοριακή μάζα νικελίου
ΟΡΙΣΜΟΣ
Σχετική μοριακή μάζα της ουσίας (Mr)είναι ένας αριθμός που δείχνει πόσες φορές η μάζα ενός δεδομένου μορίου είναι μεγαλύτερη από το 1/12 της μάζας ενός ατόμου άνθρακα, και σχετική ατομική μάζα ενός στοιχείου (A r)- πόσες φορές η μέση μάζα των ατόμων χημικό στοιχείοπερισσότερο από το 1/12 της μάζας ενός ατόμου άνθρακα.
Δεδομένου ότι στην ελεύθερη κατάσταση το νικέλιο υπάρχει με τη μορφή μονατομικών μορίων Ni, οι τιμές του ατομικού και μοριακό βάροςταιριάξει. Είναι ίσα με 58,6934.
Ισότοπα νικελίου
Είναι γνωστό ότι στη φύση το νικέλιο μπορεί να βρεθεί με τη μορφή πέντε σταθερών ισοτόπων 58 Ni, 60 Ni, 61 Ni, 62 Ni και 64 Ni. Οι μάζες τους είναι 58, 60, 61, 62 και 64, αντίστοιχα. Ο πυρήνας ενός ατόμου του ισοτόπου νικελίου 58 Ni περιέχει είκοσι οκτώ πρωτόνια και τριάντα νετρόνια και τα υπόλοιπα ισότοπα διαφέρουν από αυτόν μόνο στον αριθμό των νετρονίων.
Υπάρχουν τεχνητά ασταθή ισότοπα νικελίου με αριθμούς μάζας από 48 έως 78, καθώς και οκτώ μετα σταθερές πολιτείες, μεταξύ των οποίων το μακροβιότερο ισότοπο 59 Ni με χρόνο ημιζωής 76 χιλιάδες χρόνια.
Ιόντα νικελίου
Ο ηλεκτρονικός τύπος που δείχνει την τροχιακή κατανομή των ηλεκτρονίων νικελίου είναι ο ακόλουθος:
1s 2 2s 2 2p 6 3s 2 3p 6 3d 8 4s 2 .
Σαν άποτέλεσμα χημική αλληλεπίδρασηΤο νικέλιο εγκαταλείπει τα ηλεκτρόνια του σθένους, δηλ. είναι ο δότης τους και μετατρέπεται σε θετικά φορτισμένο ιόν:
Ni 0 -2e → Ni 2+ ;
Ni 0 -3e → Ni 3+ .
Μόριο και άτομο νικελίου
Στην ελεύθερη κατάσταση, το νικέλιο υπάρχει με τη μορφή μονοατομικών μορίων Ni. Ακολουθούν ορισμένες ιδιότητες που χαρακτηρίζουν το άτομο και το μόριο νικελίου:
Κράματα νικελίου
Η κύρια μάζα νικελίου χρησιμοποιείται για την παραγωγή διαφόρων κραμάτων με σίδηρο, χαλκό, ψευδάργυρο και άλλα μέταλλα. Η προσθήκη νικελίου στο χάλυβα αυξάνει τη σκληρότητα και την αντοχή του στη διάβρωση.
Τα κράματα με βάση το νικέλιο μπορούν να χωριστούν σε ανθεκτικά στη θερμότητα (nimonic, inconel, hastell [πάνω από 60% νικέλιο, 15-20% χρώμιο και άλλα μέταλλα]), μαγνητικά (permalloy) και κράματα με ειδικές ιδιότητες (monel metal, nickel, konstantan , invar, πλατινίτης).
Παραδείγματα επίλυσης προβλημάτων
ΠΑΡΑΔΕΙΓΜΑ 1
| Ασκηση | Γράψτε τις εξισώσεις αντίδρασης που μπορούν να χρησιμοποιηθούν για να πραγματοποιηθούν οι ακόλουθοι μετασχηματισμοί: NiCl 2 → Ni → NiSO 4 → Ni (NO 3) 2 → Ni (OH) 2 → NiCl 2. Σχεδιάστε τις εξισώσεις για τις αντιδράσεις που συμβαίνουν σε διαλύματα σε ιοντική και συντετμημένη ιοντική μορφή. |
| Απάντηση | Τοποθετώντας ένα μέταλλο πιο ενεργό από το νικέλιο σε διάλυμα χλωριούχου νικελίου (II), μπορείτε να αποκτήσετε νικέλιο σε ελεύθερη μορφή (αντίδραση υποκατάστασης): NiCl 2 + Zn → Ni + ZnCl 2; Ni 2+ + Zn 0 → Ni 0 + Zn 2+ . Το νικέλιο διαλύεται σε αραιό θειικό οξύ για να σχηματίσει θειικό νικέλιο (II): Ni + H 2 SO 4 (αραιό) → NiSO 4 + H 2; Ni 0 + 2H + → Ni 2+ + H2. Το νιτρικό νικέλιο (II) μπορεί να ληφθεί με μια αντίδραση ανταλλαγής: NiSO 4 + Ba(NO 3) 2 → Ni(NO 3) 2 + BaSO 4 ↓; SO 4 2- + Ba 2+ → BaSO 4 ↓. Με την επεξεργασία του νιτρικού νικελίου (II) με αλκάλια, μπορείτε να λάβετε υδροξείδιο του νικελίου (II): Ni(NO 3) 2 + 2NaOH → Ni(OH) 2 ↓+ 2NaNO 3; Ni 2+ + 2OH - = Ni(OH) 2 ↓. Το χλωριούχο νικέλιο (II) από το υδροξείδιο του νικελίου (II) μπορεί να ληφθεί με αντίδραση εξουδετέρωσης με υδροχλωρικό οξύ: Ni(OH) 2 + 2HCl → NiCl2 + 2H2O; OH - + H + = H 2 O. |
ΠΑΡΑΔΕΙΓΜΑ 2
| Ασκηση | Ποια μάζα χλωριούχου νικελίου (II) μπορεί να ληφθεί με θέρμανση 17,7 g νικελίου και 12 λίτρων χλωρίου (n.s.); Τι όγκος διαλύματος 0,06 Μ μπορεί να παρασκευαστεί από αυτή τη μάζα αλατιού; |
| Λύση | Ας γράψουμε την εξίσωση αντίδρασης: Ni + Cl 2 = NiCl 2. Ας βρούμε τον αριθμό των γραμμομορίων νικελίου ( μοριακή μάζα- 59 g/mol) και χλώριο που αντέδρασαν χρησιμοποιώντας τα δεδομένα που καθορίζονται στη δήλωση προβλήματος: n (Ni) = m (Ni) / M (Ni); n(Ni) = 17,7 / 59 = 0,3 mol. n (Cl2) = V (Cl2) / V m; n (Cl2) = 12 / 22,4 = 0,54 mol. Σύμφωνα με την εξίσωση του προβλήματος n (Ni): n (Cl 2) = 1:1. Αυτό σημαίνει ότι το χλώριο είναι σε περίσσεια και όλοι οι περαιτέρω υπολογισμοί πρέπει να γίνονται με χρήση νικελίου. Ας βρούμε την ποσότητα της ουσίας και τη μάζα του χλωριούχου νικελίου (II) που σχηματίστηκε (μοριακή μάζα 130 g/mol): n (Ni): n (NiCl 2) = 1:1; n (Ni) = n (NiCl 2) = 0,3 mol. m (NiCl 2) = n (NiCl 2) × M (NiCl 2); m (NiCl 2) = 0,3 × 130 = 39 g. Ας υπολογίσουμε τον όγκο ενός διαλύματος 0,06 M που μπορεί να ληφθεί από 39 g χλωριούχου νικελίου (II): V(NiCl2) = n (NiCl2)/c (NiCl2); V (NiCl 2) = 0,3 / 0,06 = 0,5 λίτρο. |
| Απάντηση | Η μάζα του χλωριούχου νικελίου (II) είναι 39 g, ο όγκος ενός διαλύματος 0,06 Μ είναι 0,5 l (500 ml). |
με θέμα: Το νικέλιο και οι ιδιότητές του
Η εργασία συντάχθηκε από μαθητές του 2ου έτους της ομάδας 5202
Nikitin Dmitry και Sharkhemullin Emil.
Καζάν 2013
Φυσικές ιδιότητες του Νικελίου.
Το στοιχείο ανακαλύφθηκε το 1761. Το νικέλιο είναι στοιχείο της δέκατης ομάδας, της τέταρτης περιόδου του περιοδικού πίνακα των χημικών στοιχείων. I. Mendeleev, με ατομικό αριθμό 28. Ασημόλευκο μέταλλο που δεν αμαυρώνει στον αέρα. Στην καθαρή του μορφή είναι πολύ πλαστικό και επιδέχεται επεξεργασία πίεσης. Είναι σιδηρομαγνητικό, δηλ. Όταν το ρεύμα διέρχεται από αυτό, παρουσιάζει έντονες μαγνητικές ιδιότητες. Τα άτομα νικελίου έχουν εξωτερική ηλεκτρονική διαμόρφωση 3d 8 4s 2. Είναι ένα εύπλαστο και εύπλαστο μέταλλο, το οποίο καθιστά δυνατή την παραγωγή των λεπτότερων φύλλων και σωλήνων από αυτό.
Χημικές ιδιότητες του Νικελίου
Χημικά, το Ni είναι παρόμοιο με το Fe και το Co, αλλά και με το Cu και τα ευγενή μέταλλα. Στις ενώσεις εμφανίζει μεταβλητό σθένος (συχνότερα 2-βαλεντένιο). Το νικέλιο είναι μέταλλο μέσης δραστικότητας. Απορροφά (ειδικά σε λεπτά διαιρεμένη κατάσταση) μεγάλες ποσότητες αερίων
Το νικέλιο καίγεται μόνο σε μορφή σκόνης. Σε αυτή την περίπτωση, σχηματίζει δύο οξείδια NiO και Ni 2 O 3 και, κατά συνέπεια, δύο υδροξείδια Ni(OH) 2 και Ni(OH) 3. Τα πιο σημαντικά διαλυτά άλατα νικελίου είναι το οξικό, το χλωριούχο, το νιτρικό και το θειικό. Τα υδατικά διαλύματα αλάτων έχουν συνήθως πράσινο χρώμα και τα άνυδρα άλατα είναι κίτρινα ή καστανοκίτρινα. , το οποίο χρησιμοποιείται συχνά στην αναλυτική χημεία.
κορεσμός του Ν. με αέρια επιδεινώνει τις μηχανικές του ιδιότητες. Η αλληλεπίδραση με το οξυγόνο ξεκινά στους 500 °C. σε λεπτή διασπορά, το Ν. είναι πυροφορικό - αναφλέγεται αυθόρμητα στον αέρα. Από τα οξείδια, το πιο σημαντικό είναι το οξείδιο του NiO - πρασινωποί κρύσταλλοι, πρακτικά αδιάλυτοι στο νερό (ορυκτός βουνσενίτης). Το υδροξείδιο κατακρημνίζεται από διαλύματα αλάτων νικελίου όταν προστίθενται αλκάλια με τη μορφή ογκώδους πράσινου ιζήματος. Όταν θερμαίνεται, το Ν συνδυάζεται με αλογόνα, σχηματίζοντας NiX 2 . Καίγοντας σε ατμούς θείου, παράγει θειούχο, παρόμοιο σε σύνθεση με το Ni 3 S 2. Το μονοσουλφίδιο NiS μπορεί να παρασκευαστεί με θέρμανση NiO με θείο. Το άζωτο δεν αντιδρά με το άζωτο ακόμη και σε υψηλές θερμοκρασίες (έως 1400 °C)
Στην υγρή κατάσταση, το Ν. διαλύει μια αξιοσημείωτη ποσότητα C, η οποία καθιζάνει κατά την ψύξη με τη μορφή γραφίτη. Όταν ο γραφίτης απελευθερώνεται, το Ν. χάνει την ελαττότητά του και την ικανότητά του να υφίσταται επεξεργασία υπό πίεση.
Το νικέλιο είναι ανθεκτικό στο νερό. Τα οργανικά οξέα δρουν στο Ν. μόνο μετά από παρατεταμένη επαφή με αυτό. Το θειικό και το υδροχλωρικό οξύ διαλύουν αργά το Ν. αραιωμένο άζωτο - πολύ εύκολο. Το συμπυκνωμένο HNO 3 παθητικοποιεί το άζωτο, αλλά σε μικρότερο βαθμό από τον σίδηρο. Όταν αλληλεπιδρούν με οξέα, σχηματίζονται άλατα δισθενούς Ni. Σχεδόν όλα τα άλατα Ni(II) και ισχυρά οξέαΕίναι πολύ διαλυτά στο νερό, τα διαλύματά τους είναι όξινα λόγω της υδρόλυσης.
Σύνθετες ενώσεις νικελίου.
Η σύνδεση του νικελίου σε σύμπλοκα είναι μια σημαντική διαγνωστική διαδικασία για την αναλυτική χημεία.
Το νικέλιο χαρακτηρίζεται από το σχηματισμό συμπλεγμάτων. Έτσι, το κατιόν Ni 2+ σχηματίζει ένα σύμπλοκο εξααμίνης 2+ και ένα σύμπλοκο διακουτετρααμίνης 2+ με αμμωνία. Αυτά τα σύμπλοκα με ανιόντα σχηματίζουν μπλε ή ιώδεις ενώσεις.
Τα αδιάλυτα άλατα περιλαμβάνουν οξαλικό και φωσφορικό (πράσινο χρώμα), τρία σουλφίδια: NiS (μαύρο), Ni 3 S 2 (κιτρινωπό-χάλκινο) και Ni 3 S 4 (ασημί-λευκό). Ή, διμεθυλγλυκοξιμικό νικέλιο Ni(C 4 H 6 N 2 O 2) 2, που δίνει ένα καθαρό κόκκινο χρώμα σε όξινο περιβάλλον, που χρησιμοποιείται ευρέως στην ποιοτική ανάλυση για την ανίχνευση του νικελίου.
Τα υδατικά διαλύματα αλάτων νικελίου (II) περιέχουν ιόν εξαακουανικελίου (II) 2+. Όταν ένα διάλυμα αμμωνίας προστίθεται σε ένα διάλυμα που περιέχει αυτά τα ιόντα, το υδροξείδιο του νικελίου (II), μια πράσινη, ζελατινώδης ουσία, κατακρημνίζεται. Αυτό το ίζημα διαλύεται όταν προστίθεται περίσσεια αμμωνίας λόγω του σχηματισμού ιόντων εξαμιννικελίου (II) 2+.
Το νικέλιο σχηματίζει σύμπλοκα με τετραεδρικές και επίπεδες τετράγωνες δομές. Για παράδειγμα, το σύμπλοκο τετραχλωρονικελικού (II)2− έχει τετραεδρική δομή, ενώ το σύμπλοκο τετραχλωρονικοιλικού (II)2− έχει επίπεδη τετράγωνη δομή.
Μια χαρακτηριστική αντίδραση ιόντων Ni 2+ με διμεθυλγλυκοξίμη οδηγεί στον σχηματισμό ροζ-κόκκινου διμεθυλγλυοξιμικού νικελίου. Αυτή η αντίδραση χρησιμοποιείται για τον ποσοτικό προσδιορισμό του νικελίου και το προϊόν της αντίδρασης χρησιμοποιείται ως χρωστική ουσία σε καλλυντικά υλικά και για άλλους σκοπούς.
Ποσοτικοποίηση ενός Στοιχείου.
Πραγματοποιείται κυρίως με τις ακόλουθες μεθόδους:
1) Κατακρήμνιση με τη μορφή διμεθοϊγλυοξιμικού νικελίου, όπως ήδη αναφέρθηκε.
2) καθίζηση με τη μορφή ενικελίου-άλφα-βενζυλοδιοξίμης.
3) Καθίζηση με τη μορφή υδροξειδίου του νικελίου (3). Αυτή η αντίδραση πραγματοποιείται χρησιμοποιώντας καυστική ποτάσα και βρωμιούχο νερό.
4) Καθίζηση ως σουλφίδιο. Πού θα χρησιμοποιηθεί το οξείδιο του νικελίου ως μορφή βάρους2.
5) Ηλεκτρολυτική μέθοδος
6) Με ογκομετρική μέθοδο - δηλαδή τιτλοδότηση του κυανιούχου καλίου μέχρι το σχηματισμό συμπλόκου κυανιδίου (Κάλιο 2 νικέλιο κυάνιο τέσσερις φορές)
7) Κολομετρική μέθοδος που βασίζεται σε μια αλλαγή στο χρώμα του ιόντος εξααμμίνης-νικελίου ή στο κόκκινο χρώμα μιας διαλυτής σύμπλοκης ένωσης, η οποία σχηματίζεται από την αντίδραση ιόντων νικελίου 3 με διμεθυλγλυοξίμη σε αλκαλικό διάλυμα παρουσία οξειδωτικού μέσο.
8) Συμπλοκομετρική μέθοδος.
ΒΑΡΥΜΕΤΡΙΚΗ ΜΕΘΟΔΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΥ ΝΙΚΕΛΙΟΥ Η μέθοδος βασίζεται στην κατακρήμνιση νικελίου σε διάλυμα αμμωνίας με διμεθυλγλυοξίμη με τη μορφή μιας ελάχιστα διαλυτής ενδοσύνθετης ένωσης παρουσία κιτρικού ή τρυγικού οξέος.
ΤΙΤΡΟΜΕΤΡΙΚΗ ΜΕΘΟΔΟΣ ΠΡΟΣΔΙΟΡΙΣΜΟΥ ΝΙΚΕΛΙΟΥ
Η μέθοδος βασίζεται στην κατακρήμνιση νικελίου σε διάλυμα αμμωνίας με διμεθυλγλυοξίμη με τη μορφή μιας ελάχιστα διαλυτής ενδοσυμπλοκής ένωσης παρουσία κιτρικού ή τρυγικού οξέος και στον προσδιορισμό του νικελίου με συμπλεκτομετρική τιτλοδότηση με το μαύρο Τ εριοχρωμίου ως δείκτη.
Ιστορία
Το νικέλιο (αγγλικά, γαλλικά και γερμανικά νικέλιο) ανακαλύφθηκε το 1751. Ωστόσο, πολύ πριν από αυτό, οι Σάξονες ανθρακωρύχοι γνώριζαν καλά το μετάλλευμα, το οποίο έμοιαζε με μετάλλευμα χαλκού και χρησιμοποιήθηκε στην κατασκευή γυαλιού για να χρωματίσει το γυαλί σε πράσινο χρώμα. Όλες οι προσπάθειες για την απόκτηση χαλκού από αυτό το μετάλλευμα ήταν ανεπιτυχείς, και ως εκ τούτου τέλη XVII V. Το μετάλλευμα ονομάστηκε Kupfernickel, που σημαίνει χονδρικά «χάλκινος διάβολος». Αυτό το μετάλλευμα (κόκκινος πυρίτης νικελίου NiAs) μελετήθηκε από τον Σουηδό ορυκτολόγο Kronstedt το 1751. Κατάφερε να αποκτήσει πράσινο οξείδιο και, μειώνοντας το τελευταίο, ένα νέο μέταλλο που ονομάζεται νικέλιο. Όταν ο Bergman έλαβε το μέταλλο σε καθαρότερη μορφή, διαπίστωσε ότι οι ιδιότητες του μετάλλου ήταν παρόμοιες με το σίδηρο. Το νικέλιο έχει μελετηθεί λεπτομερέστερα από πολλούς χημικούς, ξεκινώντας από τον Προυστ. Το Nikkel είναι μια βρώμικη λέξη στη γλώσσα των ανθρακωρύχων. Σχηματίστηκε από μια παραφθορά του Nicolaus, μια γενική λέξη που είχε πολλές σημασίες. Αλλά κυρίως η λέξη Νικόλαος χρησίμευε για να χαρακτηρίσει τους διπρόσωπους. Επιπλέον, σήμαινε «άτακτο πνευματάκι», «παραπλανητικός αργόσχολος» κ.λπ. Στη ρωσική λογοτεχνία αρχές XIX V. χρησιμοποιήθηκαν τα ονόματα Nikolan (Scherer, 1808), Nikolan (Zakharov, 1810), nicol και nickel (Dvigubsky, 1824).
Φυσικές ιδιότητες
Το μεταλλικό νικέλιο έχει ασημί χρώμα με κιτρινωπή απόχρωση, είναι πολύ σκληρό, σκληρό και εύπλαστο, γυαλίζει καλά, έλκεται από μαγνήτη, εμφανίζει μαγνητικές ιδιότητεςσε θερμοκρασίες κάτω των 340 °C.
Χημικές ιδιότητες
Διχλωριούχο νικέλιο (NiCl2)
Τα άτομα νικελίου έχουν εξωτερική διαμόρφωση ηλεκτρονίων 3d84s2. Η πιο σταθερή κατάσταση οξείδωσης για το νικέλιο είναι το Ni(II).
Το νικέλιο σχηματίζει ενώσεις με καταστάσεις οξείδωσης +2 και +3. Σε αυτή την περίπτωση, το νικέλιο με κατάσταση οξείδωσης +3 είναι διαθέσιμο μόνο με τη μορφή σύνθετων αλάτων. Για ενώσεις νικελίου +2 είναι γνωστό ένας μεγάλος αριθμός απόσυνηθισμένες και σύνθετες ενώσεις. Το οξείδιο του νικελίου Ni2O3 είναι ένας ισχυρός οξειδωτικός παράγοντας.
Το νικέλιο χαρακτηρίζεται από υψηλή αντοχή στη διάβρωση - είναι σταθερό στον αέρα, το νερό, τα αλκάλια και μια σειρά από οξέα. Η χημική αντοχή οφείλεται στην τάση του για παθητικοποίηση - το σχηματισμό ενός πυκνού φιλμ οξειδίου στην επιφάνειά του, το οποίο έχει προστατευτική δράση. Το νικέλιο διαλύεται ενεργά στο νιτρικό οξύ.
Με το μονοξείδιο του άνθρακα CO, το νικέλιο σχηματίζει εύκολα το πτητικό και εξαιρετικά τοξικό καρβονύλιο Ni(CO)4.
Η λεπτή σκόνη νικελίου είναι πυροφορική (αυτοαναφλέγεται στον αέρα).
Το νικέλιο καίγεται μόνο σε μορφή σκόνης. Σχηματίζει δύο οξείδια NiO και Ni2O3 και, κατά συνέπεια, δύο υδροξείδια Ni(OH)2 και Ni(OH)3. Τα πιο σημαντικά διαλυτά άλατα νικελίου είναι το οξικό, το χλωριούχο, το νιτρικό και το θειικό. Τα διαλύματα έχουν συνήθως πράσινο χρώμα και τα άνυδρα άλατα είναι κίτρινα ή καστανοκίτρινα. Τα αδιάλυτα άλατα περιλαμβάνουν οξαλικό και φωσφορικό (πράσινο), τρία σουλφίδια NiS (μαύρο), Ni2S3 (κιτρινωπό-χάλκινο) και Ni3S4 (μαύρο). Το νικέλιο σχηματίζει επίσης πολυάριθμες ενώσεις συντονισμού και πολύπλοκων ενώσεων. Για παράδειγμα, το διμεθυλγλυοξιμικό νικέλιο Ni(C4H6N2O2)2, το οποίο δίνει ένα καθαρό κόκκινο χρώμα σε όξινο περιβάλλον, χρησιμοποιείται ευρέως στην ποιοτική ανάλυση για την ανίχνευση του νικελίου.
Υδατικό διάλυμαΤο θειικό νικέλιο στο βάζο είναι πράσινο.
Τα υδατικά διαλύματα αλάτων νικελίου (II) περιέχουν ιόν εξαακουανικελίου (II) 2+. Όταν ένα διάλυμα αμμωνίας προστίθεται σε ένα διάλυμα που περιέχει αυτά τα ιόντα, το υδροξείδιο του νικελίου (II), μια πράσινη, ζελατινώδης ουσία, κατακρημνίζεται. Αυτό το ίζημα διαλύεται όταν προστίθεται περίσσεια αμμωνίας λόγω του σχηματισμού ιόντων εξαμιννικελίου (II) 2+.
Το νικέλιο σχηματίζει σύμπλοκα με τετραεδρικές και επίπεδες τετράγωνες δομές. Για παράδειγμα, το σύμπλοκο τετραχλωρονικελικού (II)2− έχει τετραεδρική δομή, ενώ το σύμπλοκο τετραχλωρονικοιλικού (II)2− έχει επίπεδη τετράγωνη δομή.
Η ποιοτική και ποσοτική ανάλυση χρησιμοποιεί ένα αλκαλικό διάλυμα διοξίμης βουτανοδιόνης, επίσης γνωστό ως διμεθυλγλυοξίμη, για την ανίχνευση ιόντων νικελίου (II). Όταν αντιδρά με ιόντα νικελίου(II), σχηματίζεται η ερυθρή ένωση δις(βουτανοδιοδιοξιματο)νικελίου(II). Είναι μια χηλική ένωση και ο συνδέτης διοξιμικής βουτανοδιόνης είναι δισχιδής.
Όντας στη φύση
Το νικέλιο είναι αρκετά κοινό στη φύση - το περιεχόμενό του είναι φλοιός της γηςείναι περίπου. 0,01% (μάζα). Βρίσκεται στον φλοιό της γης μόνο σε δεσμευμένη μορφή οι μετεωρίτες σιδήρου περιέχουν αυτοφυές νικέλιο (έως και 8%). Η περιεκτικότητά του στα υπερμαφικά πετρώματα είναι περίπου 200 φορές μεγαλύτερη από ό,τι στα όξινα πετρώματα (1,2 kg/t και 8 g/t). Στα υπερμαφικά πετρώματα, η κυρίαρχη ποσότητα νικελίου σχετίζεται με ολιβίνες που περιέχουν 0,13 - 0,41% Ni. Αντικαθιστά ισομορφικά το σίδηρο και το μαγνήσιο. Ένα μικρό μέρος του νικελίου υπάρχει με τη μορφή σουλφιδίων. Το νικέλιο παρουσιάζει σιδεροφιλικές και χαλκοφιλικές ιδιότητες. Με αυξημένη περιεκτικότητα σε θείο στο μάγμα, εμφανίζονται θειούχα νικέλιο μαζί με χαλκό, κοβάλτιο, σίδηρο και πλατινοειδή. Στην υδροθερμική διεργασία, μαζί με το κοβάλτιο, το αρσενικό και το θείο και μερικές φορές με το βισμούθιο, το ουράνιο και τον άργυρο, το νικέλιο σχηματίζει αυξημένες συγκεντρώσεις με τη μορφή αρσενιδίων και σουλφιδίων του νικελίου. Το νικέλιο βρίσκεται συνήθως σε θειούχα και αρσενικά μεταλλεύματα χαλκού-νικελίου.
* νικέλιο (κόκκινος νικελοπυρίτης, cupfernickel) NiAs
* χλωραντίτης (λευκός νικελοπυρίτης) (Ni, Co, Fe)As2
* γαρνιερίτης (Mg, Ni)6(Si4O11)(OH)6*H2O και άλλα πυριτικά
* μαγνητικός πυρίτης (Fe, Ni, Cu)S
* λάμψη αρσενικού-νικελίου (gersdorffite) NiAsS,
* πεντλανδίτης (Fe,Ni)9S8
Στα φυτά, κατά μέσο όρο, 5 × 10−5 τοις εκατό κατά βάρος νικελίου, στα θαλάσσια ζώα - 1,6 × 10−4, στα χερσαία ζώα - 1 × 10−6, σε ανθρώπινο σώμα— 1…2×10−6. Πολλά είναι ήδη γνωστά για το νικέλιο στους οργανισμούς. Έχει διαπιστωθεί, για παράδειγμα, ότι η περιεκτικότητά του στο ανθρώπινο αίμα αλλάζει με την ηλικία, ότι στα ζώα αυξάνεται η ποσότητα του νικελίου στο σώμα και, τέλος, ότι υπάρχουν ορισμένα φυτά και μικροοργανισμοί - «συγκεντρωτές» νικελίου, που περιέχουν χιλιάδες και μάλιστα εκατοντάδες χιλιάδες φορές περισσότερο νικέλιο από το περιβάλλον.
Κοιτάσματα μεταλλευμάτων νικελίου
Τα κύρια κοιτάσματα μεταλλευμάτων νικελίου βρίσκονται στον Καναδά, τη Ρωσία, τη Νέα Καληδονία, τις Φιλιππίνες, την Ινδονησία, την Κίνα, τη Φινλανδία και την Αυστραλία. Φυσικά ισότοπα νικελίου.
Το φυσικό νικέλιο περιέχει 5 σταθερά ισότοπα: 58Ni (68,27%), 60Ni (26,10%), 61Ni (1,13%), 62Ni (3,59%), 64Ni (0,91%).
Παραλαβή
Τα συνολικά αποθέματα νικελίου σε μεταλλεύματα στις αρχές του 1998 υπολογίζονται σε 135 εκατομμύρια τόνους, συμπεριλαμβανομένων των αξιόπιστων αποθεμάτων 49 εκατομμυρίων τόνων.
Τα κύρια μεταλλεύματα νικελίου - νικέλιο (kupfernickel) NiAs, μιλερίτης NiS, πενταλαντίτης (FeNi)9S8 - περιέχουν επίσης αρσενικό, σίδηρο και θείο. Ο πυριγενής πυρροτίτης περιέχει επίσης εγκλείσματα πενταλαντίτη. Άλλα μεταλλεύματα από τα οποία εξορύσσεται επίσης Ni περιέχουν ακαθαρσίες Co, Cu, Fe και Mg. Το νικέλιο είναι μερικές φορές το κύριο προϊόν της διεργασίας διύλισης, αλλά πιο συχνά λαμβάνεται ως υποπροϊόν σε άλλες διεργασίες μετάλλων. Από τα αξιόπιστα αποθέματα, σύμφωνα με διάφορες πηγές, από 40 έως 66% του νικελίου βρίσκεται σε «οξειδωμένα μεταλλεύματα νικελίου» (ONR), 33% σε θειούχα μεταλλεύματα, 0,7% σε άλλα. Από το 1997, το μερίδιο του νικελίου που παράγεται από την επεξεργασία ONR ήταν περίπου το 40% της παγκόσμιας παραγωγής. Σε βιομηχανικές συνθήκες, το OHP χωρίζεται σε δύο τύπους: μαγνήσιο και σιδηρούχο.
Τα πυρίμαχα μεταλλεύματα μαγνησίου, κατά κανόνα, υποβάλλονται σε ηλεκτρική τήξη με χρήση σιδηρονικελίου (5-50% Ni+Co, ανάλογα με τη σύνθεση της πρώτης ύλης και τα τεχνολογικά χαρακτηριστικά).
Τα πιο σιδηρούχα - λατεριτικά μεταλλεύματα επεξεργάζονται με υδρομεταλλουργικές μεθόδους με έκπλυση αμμωνίας-ανθρακικού ή θειικού οξέος σε αυτόκλειστο. Ανάλογα με τη σύνθεση των πρώτων υλών και τα υλικά που χρησιμοποιούνται τεχνολογικά σχήματα τελικά προϊόνταΟι τεχνολογίες αυτές είναι: οξείδιο νικελίου (76-90% Ni), πυροσυσσωμάτωση (89% Ni), συμπυκνώματα θειούχων διαφόρων συνθέσεων, καθώς και μεταλλικό ηλεκτρολυτικό νικέλιο, σκόνες νικελίου και κοβάλτιο.
Λιγότερο σιδηρούχα μεταλλεύματα μητρονίτη τήκονται σε ματ. Σε επιχειρήσεις πλήρους κύκλου, το πρόγραμμα περαιτέρω επεξεργασίας περιλαμβάνει μετατροπή, ματ ψήσιμο και ηλεκτρική τήξη οξειδίου του νικελίου για την παραγωγή μεταλλικού νικελίου. Στην πορεία, το ανακτηθέν κοβάλτιο απελευθερώνεται με τη μορφή μετάλλου ή/και αλάτων. Μια άλλη πηγή νικελίου: στην τέφρα άνθρακα της Νότιας Ουαλίας στην Αγγλία - έως και 78 κιλά νικελίου ανά τόνο. Η αυξημένη περιεκτικότητα σε νικέλιο σε ορισμένους άνθρακα, πετρέλαιο και σχιστόλιθο υποδηλώνει την πιθανότητα συγκέντρωσης νικελίου σε απολιθώματα οργανική ύλη. Οι λόγοι για αυτό το φαινόμενο δεν έχουν ακόμη διευκρινιστεί.
Το μεγαλύτερο μέρος του νικελίου λαμβάνεται από γαρνιερίτη και μαγνητικό πυρίτη.
1. Το πυριτικό μετάλλευμα ανάγεται με σκόνη άνθρακα σε κλιβάνους περιστροφικών σωλήνων σε σφαιρίδια σιδήρου-νικελίου (5-8% Ni), τα οποία στη συνέχεια καθαρίζονται από θείο, πυρώνονται και επεξεργάζονται με διάλυμα αμμωνίας. Μετά την οξίνιση του διαλύματος, λαμβάνεται μέταλλο από αυτό ηλεκτρολυτικά.
2. Μέθοδος καρβονυλίου (μέθοδος Mond). Πρώτον, ματ χαλκού-νικελίου λαμβάνεται από θειούχο μετάλλευμα, πάνω από το οποίο διέρχεται CO υπό υψηλή πίεση. Σχηματίζεται πολύ πτητικό τετρακαρβονυλονικέλιο, η θερμική αποσύνθεση του οποίου παράγει ένα ιδιαίτερα καθαρό μέταλλο.
3. Αλουμινοθερμική μέθοδος ανάκτησης νικελίου από οξείδιο μετάλλευμα: 3NiO + 2Al = 3Ni +Al2O3
Εφαρμογή
Κράματα
Το νικέλιο είναι η βάση των περισσότερων υπερκράματα - ανθεκτικά στη θερμότητα υλικά που χρησιμοποιούνται στην αεροδιαστημική βιομηχανία για εξαρτήματα σταθμών ηλεκτροπαραγωγής.
* Μέταλλο Monel (65 - 67% Ni + 30 - 32% Cu + 1% Mn), ανθεκτικό στη θερμότητα έως 500 °C, πολύ ανθεκτικό στη διάβρωση.
* λευκός χρυσός (για παράδειγμα, το πρότυπο 585 περιέχει 58,5% χρυσό και ένα κράμα (σύνδεση) από ασήμι και νικέλιο (ή παλλάδιο)).
* νιχρώμιο, κράμα αντοχής (60% Ni + 40% Cr);
* μόνιμο κράμα (76% Ni + 17% Fe + 5% Cu + 2% Cr), έχει υψηλή μαγνητική επιδεκτικότητα με πολύ χαμηλές απώλειες υστέρησης.
* invar (65% Fe + 35% Ni), σχεδόν δεν επιμηκύνεται όταν θερμαίνεται.
* Επιπλέον, τα κράματα νικελίου περιλαμβάνουν χάλυβες νικελίου και χρωμίου-νικελίου, ασήμι νικελίου και διάφορα κράματα αντίστασης όπως κονταντάνη, νικέλιο και μαγγανίνη.
Επινικελίωση
Η επινικελίωση είναι η δημιουργία μιας επικάλυψης νικελίου στην επιφάνεια ενός άλλου μετάλλου για την προστασία του από τη διάβρωση. Πραγματοποιείται με ηλεκτρολυτική επιμετάλλωση χρησιμοποιώντας ηλεκτρολύτες που περιέχουν θειικό νικέλιο (II), χλωριούχο νάτριο, υδροξείδιο του βορίου, επιφανειοδραστικές ουσίες και παράγοντες γυαλάδας και διαλυτές ανόδους νικελίου. Το πάχος του στρώματος νικελίου που προκύπτει είναι 12 - 36 μικρά. Η σταθερή γυαλάδα της επιφάνειας μπορεί να εξασφαλιστεί με επακόλουθη επιχρωμίωση (πάχος στρώσης χρωμίου 0,3 microns).
Η επίστρωση νικελίου χωρίς ρεύμα πραγματοποιείται σε διάλυμα μίγματος χλωριούχου νικελίου (II) και υποφωσφορώδους νατρίου παρουσία κιτρικού νατρίου:
NiCl2 + NaH2PO2 + H2O = Ni + NaH2PO3 + 2HCl
Η διαδικασία πραγματοποιείται σε pH 4 - 6 και 95 ° C.
Παραγωγή μπαταριών
Παραγωγή μπαταριών σιδήρου-νικελίου, νικελίου-καδμίου, νικελίου-ψευδαργύρου, νικελίου-υδρογόνου.
Τεχνολογίες ακτινοβολίας
Το νουκλίδιο 63Ni, που εκπέμπει σωματίδια β+, έχει χρόνο ημιζωής 100,1 χρόνια και χρησιμοποιείται στα κρυτρόνια.
Φάρμακο
* Χρησιμοποιείται στην κατασκευή συστημάτων βραχιόνων (νικελίδιο τιτανίου).
* Προσθετικά
Νομισματοκοπία
Το νικέλιο χρησιμοποιείται ευρέως στην παραγωγή νομισμάτων σε πολλές χώρες. Στις Ηνωμένες Πολιτείες, το νόμισμα των 5 λεπτών είναι γνωστό στην καθομιλουμένη ως νικέλιο.
Βιολογικός ρόλος
Βιολογικός ρόλος: το νικέλιο είναι ένα από τα ιχνοστοιχεία που είναι απαραίτητα για φυσιολογική ανάπτυξηζωντανοί οργανισμοί. Ωστόσο, λίγα είναι γνωστά για τον ρόλο του στους ζωντανούς οργανισμούς. Είναι γνωστό ότι το νικέλιο συμμετέχει σε ενζυμικές αντιδράσεις σε ζώα και φυτά. Στα ζώα, συσσωρεύεται σε κερατινοποιημένους ιστούς, ιδιαίτερα στα φτερά. Η αυξημένη περιεκτικότητα σε νικέλιο στα εδάφη οδηγεί σε ενδημικές ασθένειες - οι άσχημες μορφές εμφανίζονται στα φυτά και οι οφθαλμικές ασθένειες στα ζώα που σχετίζονται με τη συσσώρευση νικελίου στον κερατοειδή. Τοξική δόση (για αρουραίους) - 50 mg. Οι πτητικές ενώσεις νικελίου είναι ιδιαίτερα επιβλαβείς, ιδιαίτερα το τετρακαρβονυλ Ni(CO)4. Η μέγιστη επιτρεπόμενη συγκέντρωση ενώσεων νικελίου στον αέρα κυμαίνεται από 0,0002 έως 0,001 mg/m3 (για διάφορες ενώσεις).
Φυσιολογική δράση
Το νικέλιο είναι η κύρια αιτία αλλεργιών (δερματίτιδα εξ επαφής) σε μέταλλα που έρχονται σε επαφή με το δέρμα (κοσμήματα, ρολόγια, καρφιά τζιν). Η Ευρωπαϊκή Ένωση περιορίζει την περιεκτικότητα σε νικέλιο σε προϊόντα που έρχονται σε επαφή με το ανθρώπινο δέρμα.
Το καρβονύλιο του νικελίου είναι πολύ δηλητηριώδες. Η μέγιστη επιτρεπόμενη συγκέντρωση των ατμών του στον αέρα των βιομηχανικών χώρων είναι 0,0005 mg/m³.
Τον 20ο αιώνα, διαπιστώθηκε ότι το πάγκρεας είναι πολύ πλούσιο σε νικέλιο. Όταν το νικέλιο χορηγείται μετά την ινσουλίνη, η δράση της ινσουλίνης παρατείνεται και έτσι αυξάνεται η υπογλυκαιμική δραστηριότητα. Το νικέλιο επηρεάζει τις ενζυμικές διεργασίες, την οξείδωση του ασκορβικού οξέος και επιταχύνει τη μετάβαση των σουλφυδρυλικών ομάδων σε δισουλφιδικές ομάδες. Το νικέλιο μπορεί να αναστείλει τη δράση της αδρεναλίνης και να μειώσει την αρτηριακή πίεση. Η υπερβολική πρόσληψη νικελίου στο σώμα προκαλεί λεύκη. Το νικέλιο εναποτίθεται στο πάγκρεας και στους παραθυρεοειδείς αδένες.
Νικέλιο- μια απλή ουσία, ένα όλκιμο, ελατό, μεταβατικό μέταλλο ασημί-λευκού χρώματος, σε συνηθισμένες θερμοκρασίες στον αέρα καλύπτεται με μια λεπτή μεμβράνη οξειδίου. Χημικά ανενεργό. Ανήκει σε βαρέα μη σιδηρούχα μέταλλα, δεν βρίσκεται στην καθαρή του μορφή στη γη - είναι συνήθως μέρος διαφόρων μεταλλευμάτων, έχει υψηλή σκληρότητα, είναι καλά γυαλισμένο, είναι σιδηρομαγνητικό - έλκεται από μαγνήτη, Περιοδικός ΠίνακαςΟ Mendeleev χαρακτηρίζεται με το σύμβολο Ni και έχει τον 28ο σειριακό αριθμό.
Δείτε επίσης:
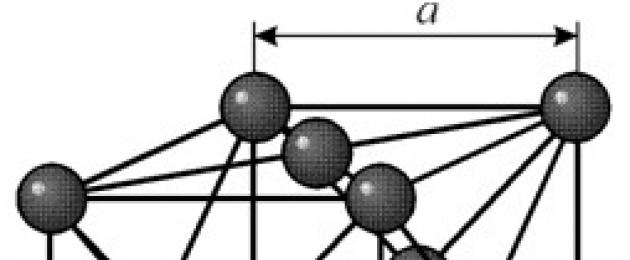
ΔΟΜΗ
 Έχει ένα επικεντρωμένο κυβικό πλέγμα με περίοδο a = 0,35238 å nm, διαστημική ομάδα Fm3m. Αυτή η κρυσταλλική δομή είναι ανθεκτική σε πίεση τουλάχιστον 70 GPa. Υπό κανονικές συνθήκες, το νικέλιο υπάρχει με τη μορφή μιας b-τροποποίησης, η οποία έχει ένα επικεντρωμένο κυβικό πλέγμα (a = 3,5236 å). Αλλά το νικέλιο που υποβάλλεται σε διάβρωση καθόδου σε ατμόσφαιρα h2 σχηματίζει μια τροποποίηση α, η οποία έχει ένα εξαγωνικό πλέγμα στενής συσκευασίας (a = 2,65 å, c = 4,32 å), το οποίο μετατρέπεται σε κυβικό πλέγμα όταν θερμαίνεται πάνω από 200 °C. Το συμπαγές κυβικό νικέλιο έχει πυκνότητα 8,9 g/cm 3 (20 °C), ατομική ακτίνα 1,24 å
Έχει ένα επικεντρωμένο κυβικό πλέγμα με περίοδο a = 0,35238 å nm, διαστημική ομάδα Fm3m. Αυτή η κρυσταλλική δομή είναι ανθεκτική σε πίεση τουλάχιστον 70 GPa. Υπό κανονικές συνθήκες, το νικέλιο υπάρχει με τη μορφή μιας b-τροποποίησης, η οποία έχει ένα επικεντρωμένο κυβικό πλέγμα (a = 3,5236 å). Αλλά το νικέλιο που υποβάλλεται σε διάβρωση καθόδου σε ατμόσφαιρα h2 σχηματίζει μια τροποποίηση α, η οποία έχει ένα εξαγωνικό πλέγμα στενής συσκευασίας (a = 2,65 å, c = 4,32 å), το οποίο μετατρέπεται σε κυβικό πλέγμα όταν θερμαίνεται πάνω από 200 °C. Το συμπαγές κυβικό νικέλιο έχει πυκνότητα 8,9 g/cm 3 (20 °C), ατομική ακτίνα 1,24 å ΙΔΙΟΤΗΤΕΣ
 Το νικέλιο είναι ένα ελατό και εύπλαστο μέταλλο που μπορεί να χρησιμοποιηθεί για την κατασκευή πολύ λεπτών φύλλων και σωλήνων. Αντοχή σε εφελκυσμό 400-500 MN/m2, όριο ελαστικότητας 80 MN/m2, αντοχή διαρροής 120 MN/m2; σχετική επιμήκυνση 40%; μέτρο κανονικής ελαστικότητας 205 Gn/m2; Σκληρότητα Brinell 600-800 Mn/m2. Στο εύρος θερμοκρασίας από 0 έως 631 Κ (το ανώτερο όριο αντιστοιχεί στο σημείο Κιουρί). Ο σιδηρομαγνητισμός του νικελίου οφείλεται στα δομικά χαρακτηριστικά των εξωτερικών κελυφών ηλεκτρονίων των ατόμων του. Το νικέλιο είναι μέρος των σημαντικότερων μαγνητικών υλικών και κραμάτων με ελάχιστο συντελεστή θερμικής διαστολής (μόνιμο κράμα, μέταλλο μονέλ, invar κ.λπ.).
Το νικέλιο είναι ένα ελατό και εύπλαστο μέταλλο που μπορεί να χρησιμοποιηθεί για την κατασκευή πολύ λεπτών φύλλων και σωλήνων. Αντοχή σε εφελκυσμό 400-500 MN/m2, όριο ελαστικότητας 80 MN/m2, αντοχή διαρροής 120 MN/m2; σχετική επιμήκυνση 40%; μέτρο κανονικής ελαστικότητας 205 Gn/m2; Σκληρότητα Brinell 600-800 Mn/m2. Στο εύρος θερμοκρασίας από 0 έως 631 Κ (το ανώτερο όριο αντιστοιχεί στο σημείο Κιουρί). Ο σιδηρομαγνητισμός του νικελίου οφείλεται στα δομικά χαρακτηριστικά των εξωτερικών κελυφών ηλεκτρονίων των ατόμων του. Το νικέλιο είναι μέρος των σημαντικότερων μαγνητικών υλικών και κραμάτων με ελάχιστο συντελεστή θερμικής διαστολής (μόνιμο κράμα, μέταλλο μονέλ, invar κ.λπ.).
ΑΠΟΘΕΜΑΤΑ ΚΑΙ ΠΑΡΑΓΩΓΗ
 Το νικέλιο είναι αρκετά κοινό στη φύση - η περιεκτικότητά του στον φλοιό της γης είναι περίπου 0,01% (κ.β.). Βρίσκεται στον φλοιό της γης μόνο σε δεσμευμένη μορφή οι μετεωρίτες σιδήρου περιέχουν αυτοφυές νικέλιο (έως και 8%). Η περιεκτικότητά του στα υπερμαφικά πετρώματα είναι περίπου 200 φορές μεγαλύτερη από ό,τι στα όξινα πετρώματα (1,2 kg/t και 8 g/t). Στα υπερμαφικά πετρώματα, η κυρίαρχη ποσότητα νικελίου σχετίζεται με ολιβίνες που περιέχουν 0,13 - 0,41% Ni.
Το νικέλιο είναι αρκετά κοινό στη φύση - η περιεκτικότητά του στον φλοιό της γης είναι περίπου 0,01% (κ.β.). Βρίσκεται στον φλοιό της γης μόνο σε δεσμευμένη μορφή οι μετεωρίτες σιδήρου περιέχουν αυτοφυές νικέλιο (έως και 8%). Η περιεκτικότητά του στα υπερμαφικά πετρώματα είναι περίπου 200 φορές μεγαλύτερη από ό,τι στα όξινα πετρώματα (1,2 kg/t και 8 g/t). Στα υπερμαφικά πετρώματα, η κυρίαρχη ποσότητα νικελίου σχετίζεται με ολιβίνες που περιέχουν 0,13 - 0,41% Ni.
Στα φυτά, κατά μέσο όρο, 5·10−5 τοις εκατό κατά βάρος νικελίου, στα θαλάσσια ζώα - 1,6·10−4, στα χερσαία ζώα - 1·10−6, στο ανθρώπινο σώμα - 1...2·10−6 .
Το μεγαλύτερο μέρος του νικελίου λαμβάνεται από γαρνιερίτη και μαγνητικό πυρίτη.
Το πυριτικό μετάλλευμα ανάγεται με σκόνη άνθρακα σε κλιβάνους περιστροφικών σωλήνων σε σφαιρίδια σιδήρου-νικελίου (5-8% Ni), τα οποία στη συνέχεια καθαρίζονται από θείο, πυρώνονται και υποβάλλονται σε επεξεργασία με διάλυμα αμμωνίας. Μετά την οξίνιση του διαλύματος, λαμβάνεται μέταλλο από αυτό ηλεκτρολυτικά.
Μέθοδος καρβονυλίου (μέθοδος Mond): Πρώτον, ματ χαλκού-νικελίου λαμβάνεται από θειούχο μετάλλευμα, πάνω από το οποίο διέρχεται CO υπό υψηλή πίεση. Σχηματίζεται πολύ πτητικό τετρακαρβονυλονικέλιο, η θερμική αποσύνθεση του οποίου παράγει ένα ιδιαίτερα καθαρό μέταλλο.
Αλουμινοθερμική μέθοδος ανάκτησης νικελίου από οξείδιο μετάλλευμα: 3NiO + 2Al = 3Ni +Al 2 O 3
ΠΡΟΕΛΕΥΣΗ
 Οι εναποθέσεις θειούχων μεταλλευμάτων χαλκού-νικελίου συνδέονται με λοπολίτες ή πλακοειδή ορεινούς όγκους πολυεπίπεδων γαββριδίων που περιορίζονται σε ζώνες βαθιάς ρηγμάτων σε αρχαίες ασπίδες και πλατφόρμες. Χαρακτηριστικό στοιχείοΤα κοιτάσματα χαλκού-νικελίου σε όλο τον κόσμο έχουν μια σταθερή σύνθεση ορυκτών μεταλλευμάτων: πυρροτίτης, πενταλαντίτης, χαλκοπυρίτης, μαγνητίτης. Εκτός από αυτά, τα μεταλλεύματα περιέχουν πυρίτη, κουβανίτη, πολυδυμίτη, νικελίτη, μιλερίτη, βιολαρίτη, ορυκτά της ομάδας πλατίνας, περιστασιακά χρωμίτη, αρσενίδια νικελίου και κοβαλτίου, γαληνίτη, φαληρίτη, βορνίτη, μακιναουίτη, βαλερίτη, γραφίτη και φυσικό χρυσό.
Οι εναποθέσεις θειούχων μεταλλευμάτων χαλκού-νικελίου συνδέονται με λοπολίτες ή πλακοειδή ορεινούς όγκους πολυεπίπεδων γαββριδίων που περιορίζονται σε ζώνες βαθιάς ρηγμάτων σε αρχαίες ασπίδες και πλατφόρμες. Χαρακτηριστικό στοιχείοΤα κοιτάσματα χαλκού-νικελίου σε όλο τον κόσμο έχουν μια σταθερή σύνθεση ορυκτών μεταλλευμάτων: πυρροτίτης, πενταλαντίτης, χαλκοπυρίτης, μαγνητίτης. Εκτός από αυτά, τα μεταλλεύματα περιέχουν πυρίτη, κουβανίτη, πολυδυμίτη, νικελίτη, μιλερίτη, βιολαρίτη, ορυκτά της ομάδας πλατίνας, περιστασιακά χρωμίτη, αρσενίδια νικελίου και κοβαλτίου, γαληνίτη, φαληρίτη, βορνίτη, μακιναουίτη, βαλερίτη, γραφίτη και φυσικό χρυσό.
Τα εξωγενή κοιτάσματα μεταλλευμάτων πυριτικού νικελίου συνδέονται παγκοσμίως με τον ένα ή τον άλλο τύπο κρούστας σερπεντενίτη που ξεπερνά τις καιρικές συνθήκες. Κατά τη διάρκεια των καιρικών συνθηκών, τα ορυκτά υφίστανται μια σταδιακή αποσύνθεση, καθώς και τη μεταφορά κινητών στοιχείων χρησιμοποιώντας νερό από άνω μέρηκρούστα προς τα κάτω. Εκεί αυτά τα στοιχεία καθιζάνουν με τη μορφή δευτερογενών ορυκτών.
Τα κοιτάσματα αυτού του τύπου περιέχουν αποθέματα νικελίου που είναι 3 φορές μεγαλύτερα από τα αποθέματά του σε θειούχα μεταλλεύματα και τα αποθέματα ορισμένων κοιτασμάτων φτάνουν το 1 εκατομμύριο τόνους νικελίου ή περισσότερο. Μεγάλα αποθέματα πυριτικών μεταλλευμάτων συγκεντρώνονται στη Νέα Καληδονία, τις Φιλιππίνες, την Ινδονησία, την Αυστραλία και άλλες χώρες. Η μέση περιεκτικότητα σε νικέλιο σε αυτά είναι 1,1-2%. Επιπλέον, τα μεταλλεύματα περιέχουν συχνά κοβάλτιο.
ΕΦΑΡΜΟΓΗ
Η συντριπτική πλειοψηφία του νικελίου χρησιμοποιείται για την παραγωγή κραμάτων με άλλα μέταλλα (fe, cr, cu, κ.λπ.), που χαρακτηρίζονται από υψηλές μηχανικές, αντιδιαβρωτικές, μαγνητικές ή ηλεκτρικές και θερμοηλεκτρικές ιδιότητες. Σε σχέση με την ανάπτυξη της τεχνολογίας jet και τη δημιουργία μονάδων αεριοστροβίλων, τα ανθεκτικά στη θερμότητα και ανθεκτικά στη θερμότητα κράματα χρωμίου-νικελίου είναι ιδιαίτερα σημαντικά. Τα κράματα νικελίου χρησιμοποιούνται σε δομές πυρηνικών αντιδραστήρων.
Σημαντικές ποσότητες νικελίου καταναλώνονται για την παραγωγή αλκαλικών μπαταριών και αντιδιαβρωτικών επικαλύψεων. Το ελατό νικέλιο στην καθαρή του μορφή χρησιμοποιείται για την κατασκευή φύλλων, σωλήνων κ.λπ. Χρησιμοποιείται επίσης σε χημική βιομηχανίαγια την κατασκευή ειδικού χημικού εξοπλισμού και ως καταλύτης για πολλές χημικές διεργασίες. Το νικέλιο είναι ένα πολύ σπάνιο μέταλλο και, αν είναι δυνατόν, θα πρέπει να αντικατασταθεί από άλλα, φθηνότερα και πιο κοινά υλικά.
Χρησιμοποιείται στην κατασκευή συστημάτων βραχιόνων (νικελίδιο τιτανίου) και προσθετικών. Χρησιμοποιείται ευρέως στην παραγωγή νομισμάτων σε πολλές χώρες. Στις Ηνωμένες Πολιτείες, το νόμισμα των 5 λεπτών είναι γνωστό στην καθομιλουμένη ως νικέλιο. Το νικέλιο χρησιμοποιείται επίσης για την κατασκευή χορδών περιέλιξης για μουσικά όργανα.
Νικέλιο - Νι
ΤΑΞΙΝΟΜΗΣΗ
| Strunz (8η έκδοση) | 1/Α.08-10 |
| Nickel-Strunz (10η έκδοση) | 1.ΑΑ.05 |
| Dana (7η έκδοση) | 1.1.17.2 |
| Dana (8η έκδοση) | 1.1.11.5 | Hey's CIM Ref | 1.61 |
Οι ιδιότητες του νικελίου είναι σημαντικές παράμετροι για την αναζήτηση, την επεξεργασία και τις εφαρμογές του μετάλλου. Λαμβάνονται υπόψη όταν σχηματίζονται συνθέσεις με άλλα υλικά.
Οι ιδιότητες του νικελίου καθορίζουν τη χρήση του στην παραγωγή
Το νικέλιο είναι ένα μέταλλο με χαρακτηριστικό ασημί-λευκό χρώμα. Σε θερμοκρασία 1453 °C μετατρέπεται σε υγρή κατάστασηκαι βράζει στους 2732 °C. Το νικέλιο είναι όλκιμο και μπορεί εύκολα να υποστεί επεξεργασία υπό πίεση.
Η χημική ιδιότητα του νικελίου χαρακτηρίζεται από την ικανότητα να σχηματίζει ενώσεις με διαφορετικούς βαθμούς οξείδωσης. Υπό φυσικές συνθήκες, εμφανίζεται ένα λεπτό φιλμ οξειδίου στην επιφάνεια του μετάλλου.
Το μέταλλο είναι ιδιαίτερα ανθεκτικό στη διάβρωση. Το νικέλιο δεν αντιδρά με πολλά πυκνά οξέα και αλκάλια, αλλά διαλύεται ενεργά σε αραιό νιτρικό οξύ.

Όταν το νικέλιο εισέρχεται σε χημικές αντιδράσεις, σχηματίζει πτητικά μέταλλα και διαλυτά/αδιάλυτα άλατα
Δεν αντιδρούν με το νικέλιο:
- αδρανή αέρια;
- λίθιο;
- κάλιο;
- νάτριο;
- καίσιο;
- ρουβίνιο;
- στρόντιο;
- βάριο;
- ιρίδιο;
- καίσιο.
Με μια ένωση άνθρακα, το νικέλιο σχηματίζει καρβονύλιο, ένα πτητικό μέταλλο μετάπτωσης που χρησιμοποιείται στη διαδικασία παραγωγής υλικών υψηλής καθαρότητας. Η σκόνη νικελίου μπορεί να αναφλεγεί αυθόρμητα όταν έρθει σε επαφή με τον αέρα, σχηματίζοντας οξείδια.
Το νικέλιο παράγει μια σειρά από διαλυτά και αδιάλυτα άλατα. Για παράδειγμα, ένα διάλυμα θειικού μετάλλου δίνει στο υγρό πράσινο χρώμα. Τα αδιάλυτα άλατα έχουν συνήθως βαθύ κίτρινο χρώμα.
Μορφές εμφάνισης μετάλλων
Υπό φυσικές συνθήκες, το νικέλιο βρίσκεται σε συνδυασμό με μια σειρά από χημικά στοιχεία, και με τη μορφή ψήγματα βρίσκεται σε μετεωρίτες σιδήρου.
Υπό υδροθερμικές συνθήκες, το νικέλιο σχηματίζει ενώσεις με αρσενικό, κοβάλτιο και άργυρο. Οι αυξημένες συγκεντρώσεις του μετάλλου συνδέονται με ορυκτούς σχηματισμούς - αρσενίδια και σουλφίδια.

Στη φύση, το νικέλιο βρίσκεται συνήθως σε ενώσεις με άλλα στοιχεία
Οι πρώτες ύλες για την εξόρυξη του πολύτιμου συστατικού είναι θειούχα, μεταλλεύματα χαλκού-νικελίου που περιέχουν αρσενικό:
- νικέλιο - μια ένωση με αρσενικό.
- Χλωαντίτης - λευκός πυρίτης που περιέχει κοβάλτιο και σίδηρο.
- γαρνιερίτης - πυριτικό πέτρωμα που περιέχει μαγνήσιο.
- μαγνητικός πυρίτης - μια ένωση θείου με σίδηρο και χαλκό.
- gersdorfit - λάμψη αρσενικού-νικελίου.
- Ο πεντλαντίτης είναι μια ένωση θείου, σιδήρου και νικελίου.
Η περιεκτικότητα σε μέταλλα στους ζωντανούς οργανισμούς εξαρτάται από τις συνθήκες και το περιβάλλον. Ορισμένοι εκπρόσωποι της χλωρίδας και της πανίδας είναι ικανοί να συγκεντρώνουν μέταλλο.
Τα κύρια κοιτάσματα μεταλλεύματος βρίσκονται στον Καναδά, Ρωσική Ομοσπονδία, Αλβανία, Νότια Αφρική, Κούβα, Ελλάδα.
Η διαδικασία εξόρυξης μετάλλου από μεταλλεύματα περιλαμβάνει τη χρήση τεχνολογιών ανάλογα με τον τύπο της πρώτης ύλης. Μερικές φορές το νικέλιο είναι ένα δευτερεύον υλικό για τον εμπλουτισμό του βράχου.
Τα πυρίμαχα μεταλλεύματα που περιέχουν μαγνήσιο υποβάλλονται σε ηλεκτρική τήξη. Τα μεταλλεύματα λατερίτη που περιέχουν σίδηρο επεξεργάζονται με την υδρομεταλλουργική μέθοδο και ακολουθεί επεξεργασία με αλκαλικά διαλύματα.
Ο βράχος με λιγότερη περιεκτικότητα σε σίδηρο λιώνει, ψήνεται και λιώνει ηλεκτρικά. Στην πορεία ανακτάται μεταλλικό κοβάλτιο ή τα άλατά του. Αυξημένη περιεκτικότητα σε μέταλλα παρατηρείται στην τέφρα άνθρακα στην Αγγλία. Το γεγονός αυτό συνδέεται με τη δραστηριότητα των μικροοργανισμών που συγκεντρώνουν το νικέλιο.
Πλαστικότητα και άλλα φυσικές ιδιότητεςΟι συνθέσεις νικελίου εξαρτώνται από την καθαρότητα του υλικού. Μια ελαφριά πρόσμιξη θείου κάνει το μέταλλο εύθραυστο. Η προσθήκη μαγνησίου στο λιωμένο υλικό καθαρίζει το μείγμα από μικρές ακαθαρσίες για να σχηματιστεί μια ένωση με θείο.
Εφαρμογές Νικελίου
Οι φυσικές και χημικές ιδιότητες του μετάλλου καθορίζουν τη χρήση του:
- στην παραγωγή ανοξείδωτου χάλυβα.
- για το σχηματισμό κραμάτων που δεν περιέχουν σίδηρο.
- για σκοπούς εφαρμογής προστατευτικών επικαλύψεων σε προϊόντα με γαλβανική μέθοδο·
- για την παραγωγή χημικών αντιδραστηρίων·
- στη μεταλλουργία σκόνης.
Το μέταλλο χρησιμοποιείται στην παραγωγή μπαταριών, με τη βοήθειά του συμβαίνουν καταλυτικές διεργασίες. χημικές αντιδράσειςστη βιομηχανική παραγωγή. Τα κράματα τιτανίου είναι εξαιρετικά υλικά για την κατασκευή οδοντοστοιχιών και συσκευών ανόρθωσης δοντιών.
Η σύνθεση που βασίζεται στο χημικό στοιχείο Νο. 28 είναι μια πρώτη ύλη για την κοπή νομισμάτων και την κατασκευή πηνίων για ηλεκτρονικά τσιγάρα. Χρησιμοποιείται για να κουρδίζει τις χορδές των μουσικών οργάνων.
Στην κατασκευή πυρήνων για ηλεκτρομαγνήτες, χρησιμοποιούνται συνθέσεις - μόνιμο κράμα, συμπεριλαμβανομένου 20–60% σιδήρου. Το νικέλιο χρησιμοποιείται στην κατασκευή διαφόρων εξαρτημάτων και εξοπλισμού για τη χημική βιομηχανία.
Τα οξείδια μετάλλων χρησιμοποιούνται στην παραγωγή γυαλιού, υαλοπινάκων και κεραμικών. Η σύγχρονη παραγωγή ειδικεύεται στην παραγωγή μιας ποικιλίας προϊόντων έλασης: σύρμα, ταινία, φύλλο, σωλήνες.

Το νικέλιο έχει ένα ευρύ φάσμα εφαρμογών από επικαλύψεις έως χημικά
Η αντίσταση σε επιθετικά περιβάλλοντα επιτρέπει τη χρήση ελασματοποιημένου νικελίου για τη μεταφορά αλκαλίων στη χημική βιομηχανία.
Τα όργανα από κράμα με βάση το νικέλιο χρησιμοποιούνται στην ιατρική και σε επιστημονική έρευνα. Το μέταλλο χρησιμοποιείται για τη δημιουργία οργάνων ακριβείας για τηλεχειριστήριοδιεργασίες στην πυρηνική ενέργεια, εγκαταστάσεις ραντάρ.
Χαρακτηριστικά κραμάτων νικελίου
Οι συνθέσεις συνδυάζουν το μέταλλο κυρίως με σίδηρο και κοβάλτιο. Χρησιμοποιείται ως συστατικό κράματος για την παραγωγή διαφόρων δομικών τύπων χάλυβα, μαγνητικών και μη μαγνητικών κραμάτων.
Τα κράματα μετάλλων με βάση το χημικό στοιχείο Νο. 28 έχουν αντοχή, αντοχή σε θερμοκρασίες, παραμόρφωση και περιβαλλοντικές επιδράσεις. Ο αριθμός τους φτάνει τις πολλές χιλιάδες. Οι πιο κοινές συνθέσεις είναι συνδυασμοί με χρώμιο, μολυβδαίνιο, αλουμίνιο, τιτάνιο και βηρύλλιο.
Το μέταλλο θεωρείται συστατικό απολίνωσης του χρυσού, δίνοντας στα κοσμήματα το χαρακτηριστικό λευκό χρώμα και τη δύναμή τους. Σε σχέση με αυτή τη σύνθεση, υπάρχουν απόψεις για την αλλεργική επίδραση του νικελίου στο δέρμα.
Σε συνδυασμό με το χρώμιο, σχηματίζεται μια ένωση νιχρώμου, η οποία είναι ανθεκτική υψηλή θερμοκρασία, ελάχιστος συντελεστής ηλεκτρικής αντίστασης, ολκιμότητα.
Χρησιμοποιείται για την κατασκευή συσκευών θέρμανσης, εξαρτημάτων και ως επίστρωση. Η υψηλή αντοχή της σύνδεσης της επιτρέπει να υποβληθεί μηχανική κατεργασία, τόρνευση, συγκόλληση, σφράγιση.

Τα κράματα νικελίου έχουν υψηλή αντοχή, γεγονός που τους επιτρέπει να χρησιμοποιούνται ευρέως στην παραγωγή
Μια ειδική ομάδα σχηματίζεται από κράματα που περιλαμβάνουν χαλκό. Μεταξύ αυτών τα πιο δημοφιλή είναι:
- Monel?
- ορείχαλκος;
- μπρούντζος;
- νικέλιο ασήμι.
Πριν από περισσότερο από έναν αιώνα, διαπιστώθηκε ότι η σύνθεση σιδήρου-νικελίου, που περιέχει 28% του περιγραφόμενου μετάλλου, χάνει τις ιδιότητες μαγνήτισής της. Τα κράματα που περιέχουν νικέλιο 36% χαρακτηρίζονται από έναν ασήμαντο γραμμικό ρυθμό διαστολής, ο οποίος τους επιτρέπει να χρησιμοποιούνται στην κατασκευή οργάνων και εργαλείων ακριβείας.
Αυτή η σύνθεση, η οποία ονομάζεται FeNi36, ονομάζεται invar, δηλαδή «αμετάβλητη». Το κράμα Kovar, που περιέχει 29% νικέλιο, 17% κοβάλτιο και 54% σίδηρο, έχει βρει ευρεία χρήση στην παραγωγή.
Έχει υψηλή πρόσφυση στο λιωμένο γυαλί, γεγονός που επιτρέπει τη χρήση της σύνθεσης για την κατασκευή ηλεκτρικών καλωδίων που διέρχονται από αυτήν την ουσία.
- Σε επαφή με 0
- Google+ 0
- Εντάξει 0
- Facebook 0