Efter att ha ställt frågan - varför behövs järnmalm, blir det klart att utan det skulle en person inte nå höjder modern utveckling civilisation. Verktyg och vapen, maskindelar och verktygsmaskiner - allt detta kan göras av järnmalm. Idag finns ingen industri nationalekonomi, utan stål eller gjutjärn.
Järn är brett distribuerat i jordskorpan kemiska grundämnen. Detta grundämne finns praktiskt taget aldrig i sin rena form i jordskorpan, det finns i form av föreningar (oxider, karbonater, salter, etc.). Mineralföreningar som innehåller betydande mängder av detta grundämne kallas järnmalm. Industriell användning av malmer som innehåller ≥ 55 % järn är ekonomiskt motiverad. Malmmaterial med lägre metallhalt är föremål för preliminär anrikning. Anrikningsmetoder för järnmalmsbrytning förbättras ständigt. Därför minskar i dagsläget ständigt kraven på mängden järn i järnmalm (dålig). Malm består av föreningar av det malmbildande grundämnet, mineralföroreningar och gråberg.
- malmer som bildas under inverkan av hög temperatur kallas magmatiska;
- bildas som ett resultat av sedimentation på botten av antika hav - exogent;
- under påverkan av extremt tryck och temperatur - metamorfogen.
Bergartens ursprung bestämmer villkoren för gruvdrift och i vilken form järn finns i dem.
Huvuddraget hos järnmalmer är deras utbredda förekomst och mycket betydande reserver i jordskorpan.
De viktigaste järnhaltiga mineralföreningarna är:
- hematit är den mest värdefulla källan till järn, eftersom den innehåller cirka 68-72% av grundämnet och ett minimum av skadliga föroreningar, hematitavlagringar kallas röd järnmalm;
- magnetit är huvudegenskapen hos denna typ av järnmalm - magnetiska egenskaper. Tillsammans med hematit har den en järnhalt på 72,5%, samt en hög svavelhalt. Bildar avlagringar - magnetiska järnmalmer;
- en grupp vattenhaltiga metalloxider som gemensamt kallas bruna järnmalmer. Dessa malmer har låg järnhalt, inblandningar av mangan och fosfor. Detta bestämmer egenskaperna hos järnmalm av denna typ - betydande reducerbarhet, porositet i strukturen;
- siderit (järnkarbonat) – har hög halt av gråberg, själva metallen innehåller ca 48%.
Järnmalmsapplikationer
Järnmalm används för att smälta gjutjärn, stålgjutjärn och stål. Men innan järnmalm används för sitt avsedda ändamål, genomgår den anrikning vid gruv- och bearbetningsanläggningar. Det gäller dåliga malmmaterial vars järnhalt är under 25-26 %. Flera metoder för anrikning av låghaltiga malmer har utvecklats:
- magnetisk metod, det innebär att man använder skillnader i den magnetiska permeabiliteten hos malmkomponenter;
- flotationsmetod, med användning av olika vätbarhetskoefficienter för malmpartiklar;
- spolningsmetod, som tar bort tomma föroreningar med vätskestrålar under högt tryck;
- gravitationsmetod, med speciella suspensioner för att avlägsna gråberg.
Som ett resultat av förädlingen erhålls ett koncentrat som innehåller upp till 66-69% metall från järnmalm.
Hur och var järnmalm och koncentrat används:
- malm används i masugnsproduktion för smältning av gjutjärn;
- att producera stål direkt, förbi gjutjärnssteget;
- för tillverkning av ferrolegeringar.
Som ett resultat tillverkas profiler och plåtar av det resulterande stålet och gjutjärnet, från vilka de nödvändiga produkterna sedan tillverkas.
En formbar, silvervit metall med hög kemisk reaktivitet: järn korroderar snabbt när det utsätts för höga temperaturer eller hög luftfuktighet. Järn brinner i rent syre, och i fint dispergerat tillstånd antänds det spontant i luften. Betecknas med symbolen Fe (latin Ferrum). En av de vanligaste metallerna i jordskorpan (andra plats efter).
Se även:
STRUKTURERA

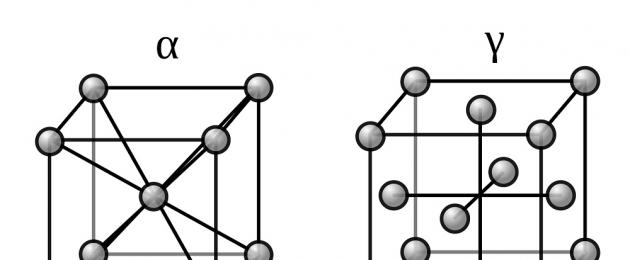
Flera polymorfa modifieringar har etablerats för järn, varav högtemperaturmodifieringen - γ-Fe (över 906°) bildar ett gitter av en ansiktscentrerad kub av Cu-typ (a 0 = 3,63), och lågtemperaturen modifiering - α-Fe-gittret av en centrerad kub av α-Fe-typ (a 0 = 2,86).
Beroende på uppvärmningstemperaturen kan järn hittas i tre modifikationer, kännetecknade av olika kristallgitterstrukturer:
- I temperaturområdet från den lägsta till 910°C - a-ferrit (alfaferrit), som har en kristallgitterstruktur i form av en centrerad kub;
- I temperaturintervallet från 910 till 1390°C - austenit, vars kristallgitter har strukturen av en ansiktscentrerad kub;
- I temperaturområdet från 1390 till 1535°C (smältpunkt) - d-ferrit (delta ferrit). Kristallgittret för d-ferrit är detsamma som för a-ferrit. Den enda skillnaden mellan dem är de olika (större för d-ferrit) avstånden mellan atomerna.
När flytande järn kyls uppstår primära kristaller (kristallisationscentra) samtidigt på många punkter i den kylda volymen. Med efterföljande kylning byggs nya kristallina celler runt varje centrum tills hela förrådet av flytande metall är slut.
Resultatet är en granulär struktur av metallen. Varje korn har ett kristallgitter med en viss riktning på sina axlar.
Med efterföljande kylning av fast järn, under övergångarna av d-ferrit till austenit och austenit till a-ferrit, kan nya kristallisationscentra uppstå med en motsvarande förändring i kornstorlek
EGENSKAPER

I sin rena form under normala förhållanden är det ett fast ämne. Den har en silvergrå färg och en uttalad metallisk lyster. De mekaniska egenskaperna hos järn inkluderar dess hårdhetsnivå på Mohs-skalan. Det är lika med fyra (genomsnitt). Järn har god elektrisk och termisk ledningsförmåga. Den sista egenskapen kan kännas genom att röra vid ett järnföremål i ett kallt rum. Eftersom detta material leder värme snabbt tar det bort det mesta från din hud på kort tid, vilket är anledningen till att du känner dig kall.
Om du rör till exempel trä kommer du att märka att dess värmeledningsförmåga är mycket lägre. De fysikaliska egenskaperna hos järn inkluderar dess smält- och kokpunkter. Den första är 1539 grader Celsius, den andra är 2860 grader Celsius. Vi kan dra slutsatsen att de karakteristiska egenskaperna hos järn är god duktilitet och smältbarhet. Men det är inte allt. De fysiska egenskaperna hos järn inkluderar också dess ferromagnetism. Vad det är? Järn, vars magnetiska egenskaper vi kan observera i praktiska exempel varje dag, är den enda metallen som har en så unik särdrag. Detta förklaras av detta material kan magnetiseras under påverkan av ett magnetfält. Och efter slutet av den senares verkan förblir järnet, vars magnetiska egenskaper just har bildats, en magnet under lång tid. Detta fenomen kan förklaras av det faktum att i strukturen av denna metall finns det många fria elektroner som kan röra sig.
RESERVER OCH PRODUKTION
Järn är ett av de vanligaste grundämnena i solsystem, särskilt på de jordiska planeterna, särskilt på jorden. En betydande del av de jordiska planeternas järn finns i planeternas kärnor, där dess innehåll uppskattas till cirka 90 %. Järnhalten i jordskorpan är 5 % och i manteln cirka 12 %.

Järn är ganska utbrett i jordskorpan - det står för cirka 4,1% av massan av jordskorpan (4:e plats bland alla element, 2:a bland metaller). I manteln och skorpan är järn koncentrerat huvudsakligen i silikater, medan dess innehåll är betydande i basiska och ultrabasiska bergarter, och lågt i sura och mellanliggande bergarter.
Ett stort antal malmer och mineraler som innehåller järn är kända. Av största praktiska betydelse är röd järnmalm (hematit, Fe2O3; innehåller upp till 70 % Fe), magnetisk järnmalm (magnetit, FeFe 2 O 4, Fe 3 O 4; innehåller 72,4 % Fe), brun järnmalm eller limonit (goetit). och hydrogoetit, FeOOH respektive FeOOH nH2O). Goetit och hydrogoetit finns oftast i vittringsskorpor och bildar så kallade "järnhattar", vars tjocklek når flera hundra meter. De kan också vara av sedimentärt ursprung och falla ur kolloidala lösningar i sjöar eller kustområden i haven. I det här fallet bildas oolitiska, eller baljväxter, järnmalmer. Vivianite Fe 3 (PO 4) 2 8H 2 O finns ofta i dem och bildar svarta långsträckta kristaller och radiella aggregat.
Järnhalt i havsvatten— 1·10 −5 -1·10 −8 %
Inom industrin utvinns järn från järnmalm, främst från hematit (Fe 2 O 3) och magnetit (FeO Fe 2 O 3).
Det finns olika sätt att utvinna järn ur malmer. Det vanligaste är domänprocessen.
Det första steget i produktionen är reduktion av järn med kol i en masugn vid en temperatur på 2000 °C. I en masugn matas kol i form av koks, järnmalm i form av agglomerat eller pellets och flussmedel (som kalksten) uppifrån och möts av en ström av påtvingad varm luft underifrån.
Förutom masugnsprocessen är processen med direkt järnframställning vanlig. I detta fall blandas förkrossad malm med speciell lera, vilket bildar pellets. Pelletsen eldas och behandlas i en schaktugn med heta metanomvandlingsprodukter, som innehåller väte. Väte reducerar lätt järn utan att förorena järnet med föroreningar som svavel och fosfor, som är vanliga föroreningar i kol. Järn erhålls i fast form och smälts därefter i elektriska ugnar. Kemiskt rent järn erhålls genom elektrolys av lösningar av dess salter.
URSPRUNG

Ursprung telluriskt (jordbundet) järn finns sällan i basaltlavor (Uifak, Disko Island, utanför Grönlands västra kust, nära Kassel, Tyskland). På båda punkterna är pyrrotit (Fe 1-x S) och kohenit (Fe 3 C) associerade med det, vilket förklaras av både reduktionen med kol (inklusive från värdbergarna) och nedbrytningen av karbonylkomplex som Fe( CO) n. I mikroskopiska korn har den mer än en gång etablerats i förändrade (serpentiniserade) ultrabasiska bergarter, även i paragenes med pyrrotit, ibland med magnetit, på grund av vilken den uppstår vid reduktionsreaktioner. Mycket sällsynt i oxidationszon malmfyndigheter, under bildandet av sumpmalmer. Fynd har registrerats i sedimentära bergarter i samband med reduktionen av järnföreningar med väte och kolväten.
Nästan rent järn hittades i månens jord, vilket är förknippat med både meteoritfall och magmatiska processer. Slutligen innehåller två klasser av meteoriter - stenigt järn och järn - naturliga järnlegeringar som en bergbildande komponent.
ANSÖKAN

Järn är en av de mest använda metallerna och står för upp till 95 % av den globala metallurgiska produktionen.
Järn är huvudkomponenten i stål och gjutjärn - de viktigaste konstruktionsmaterialen.
Järn kan ingå i legeringar baserade på andra metaller - till exempel nickel.
Magnetisk järnoxid (magnetit) är ett viktigt material i produktionen av långtidsminnesenheter för datorer: hårddiskar, disketter, etc.
Ultrafint magnetitpulver används i många svartvita laserskrivare blandat med polymergranulat som toner. Detta använder både magnetitens svarta färg och dess förmåga att fastna på den magnetiserade överföringsvalsen.
De unika ferromagnetiska egenskaperna hos ett antal järnbaserade legeringar bidrar till deras utbredda användning inom elektroteknik för magnetiska kärnor i transformatorer och elmotorer.
Järn(III)klorid (järn(III)klorid) används i amatörradiopraxis för etsning av kretskort.
Järnsulfatheptat (järnsulfat) blandat med kopparsulfat används för att bekämpa skadliga svampar i trädgårdsskötsel och konstruktion.
Järn används som anod i järn-nickel-batterier och järn-luft-batterier.
Vattenlösningar av järn- och järnklorider, såväl som dess sulfater, används som koaguleringsmedel i reningsprocesser av naturligt och avloppsvatten vid vattenbehandling av industriföretag.
Järn - Fe
KLASSIFICERING
Hejs CIM Ref1.57
| Strunz (8:e upplagan) | 1/A.07-10 |
| Nickel-Strunz (10:e upplagan) | 1.AE.05 |
| Dana (7:e upplagan) | 1.1.17.1 |
/ mineral Järn
Järn tillhör gruppen inhemska grundämnen. Naturligt järn är ett mineral av jordbundet och kosmogent ursprung. Nickelhalten är 3 procent högre i landjordiskt järn jämfört med kosmogent järn. Den innehåller även föroreningar av magnesium, kobolt och andra spårämnen. Naturligt järn har en ljusgrå färg med en metallisk lyster; inneslutningar av kristaller är sällsynta. Detta är ett ganska sällsynt mineral med en hårdhet på 4-5 enheter. och en densitet på 7000-7800 kg per kubikmeter. Arkeologer har bevisat att inhemskt järn användes av forntida människor långt innan de utvecklade färdigheterna att smälta järnmetall från malm. Denna metall i sin ursprungliga form har en silvervit nyans, ytan blir snabbt täckt av rost vid hög luftfuktighet eller i syrerikt vatten. Denna sten har god duktilitet, smälter vid en temperatur av 1530 grader Celsius och kan lätt smidas till produkter och valsas. Metallen har god elektrisk och termisk ledningsförmåga; den särskiljs dessutom från andra bergarter genom sina magnetiska egenskaper. När den interagerar med syre täcks metallens yta med den resulterande filmen, vilket skyddar den från frätande effekter. Och när det finns fukt i luften oxiderar järn och rost bildas på dess yta. I vissa syror löses järn och väte frigörs. Järn hade en enorm inverkan på utvecklingen Mänskligt samhälle och fortsätter att värderas idag. Det används i många branscher. Järn hjälpte primitiva människan att bemästra nya jaktmetoder och ledde till utvecklingen Lantbruk tack vare nya verktyg. Rent järn på den tiden var en del av fallna meteoriter. Till denna dag finns det legender om det överjordiska ursprunget till detta material. Metallurgin går tillbaka till mitten av det andra årtusendet f.Kr. På den tiden behärskade Egypten produktionen av metall från järnmalm. I sin rena form finns järn i himlakroppar. Metallen upptäcktes i månens jord. Nu bryts järn från stenmalm, och Ryssland har en ledande position i utvinningen av denna metall. Rika fyndigheter av järnmalm finns i den europeiska delen, i Västra Sibirien och i Ural. Järn är viktigt vid tillverkning av stål, som har ett brett användningsområde. Detta material används i nästan varje produktion. Järn används ofta i vardagen, det kan hittas i form av smidda produkter och gjutjärn. Järn låter dig ge produkten olika former, så det används i smide och skapa lusthus, staket och andra produkter. Alla hemmafruar använder järn i köket, eftersom produkter gjorda av gjutjärn inte är något annat än en legering av järn och kol. Kokkärl i gjutjärn värms upp jämnt, håller temperaturen under lång tid och håller i årtionden. Nästan allt bestick innehåller järn, och rostfritt stål används för att göra tallrikar och olika köksredskap och sådana nödvändiga föremål som spadar, gafflar, yxor och andra användbara redskap. Denna metall används också flitigt i smycken. Telluriskt järn innehåller föroreningar av nickel (Ni) 0,6-2 %, kobolt (Co) upp till 0,3 %, koppar (Cu) upp till 0,4 %, platina (Pt) upp till 0,1 %, kol; i meteoritjärn varierar nickel från 2 till 12 %, kobolt är cirka 0,5 %, och det finns också föroreningar av fosfor, svavel och kol. Beteende i syror: löses i HNO3. Inhemsk järnfamilj (enligt Godovikov) Native Nickel Group Järn (engelska järn, franska Fer, tyska Eisen) är en av antikens sju metaller. Det är mycket troligt att människan blev bekant med järn av meteorit ursprung tidigare än med andra metaller. Meteoriskt järn är vanligtvis lätt att skilja från markjärn, eftersom det nästan alltid innehåller från 5 till 30% nickel, oftast 7-8%. Sedan urminnes tider har man fått järn från malmer som förekommer nästan överallt. De vanligaste malmerna är hematit (Fe 2 O 3,), brun järnmalm (2Fe 2 O 3, ZN 2 O) och dess varianter (sumpmalm, siderit eller sparjärn FeCO3,), magnetit (Fe 3 0 4) och några andra. Alla dessa malmer, när de värms upp med kol, reduceras lätt vid en relativt låg temperatur, med början från 500 o C. Den resulterande metallen hade utseendet av en trögflytande svampig massa, som sedan bearbetades vid 700-800 o Med upprepad smidning. I antiken och medeltiden jämfördes de sju då kända metallerna med de sju planeterna, som symboliserade sambandet mellan metaller och himlakroppar och metallernas himmelska ursprung. Denna jämförelse blev vanlig för mer än 2000 år sedan och återfinns ständigt i litteraturen fram till 1800-talet. Under II-talet. n. e. järn jämfördes med Merkurius och kallades kvicksilver, men senare började det jämföras med Mars och kallas Mars, vilket särskilt betonade den yttre likheten mellan Mars rödaktiga färg och röda järnmalmer.Järnets historia
Var bryts järn?
Användningsområden
Kemisk sammansättning
I naturen finns det flera modifieringar av järn - den lågtemperaturscell har en bcc-cell (Im3m), högtemperaturen (vid temperaturer > 1179K) fcc-cellen (Fm(-3)m). Finns i stora mängder i meteoriter. Widmanstätten-figurer förekommer i järnmeteoriter när de etsas eller upphettas.
Ursprung: telluriskt (jordiskt) järn finns sällan i basaltiska lavor (Uifak, Disko Island, utanför Grönlands västra kust, nära Kassel, Tyskland). På båda punkterna är pyrrotit (Fe1-xS) och kohenit (Fe3C) associerade med det, vilket förklaras av både reduktion med kol (inklusive från värdbergarterna) och nedbrytning av karbonylkomplex som Fe(CO)n. I mikroskopiska korn har den mer än en gång etablerats i förändrade (serpentiniserade) ultrabasiska bergarter, även i paragenes med pyrrotit, ibland med magnetit, på grund av vilken den uppstår vid reduktionsreaktioner. Mycket sällan finns i oxidationszonen av malmfyndigheter, under bildandet av sumpmalmer. Fynd har registrerats i sedimentära bergarter i samband med reduktionen av järnföreningar med väte och kolväten.
Nästan rent järn hittades i månens jord, vilket är förknippat med både meteoritfall och magmatiska processer. Slutligen innehåller två klasser av meteoriter - stenigt järn och järn - naturliga järnlegeringar som en bergbildande komponent.
Inhemsk järngrupp
> 24 kl. % Ni - taenit
62,5 - 92 kl. % Ni - awaruite Ni3Fe
(Ni, Fe) - Naturligt nickel
rapportera ett fel i beskrivningen
Mineralets egenskaper
| namnets ursprung | Beteckningen på det kemiska elementet kommer från latinets ferrum, järn - från det gamla engelska ordet som betyder denna metall |
| Öppningsplats | Qeqertarsuaq Island (Disko Island), Qaasuitsup, Grönland |
| Öppningsår | känt sedan urminnes tider |
| Termiska egenskaper | P. tr. Smältpunkt (rent järn) 1528°C |
| IMA-status | giltig, först beskriven före 1959 (före IMA) |
| Typiska föroreningar | Ni,C,Co,P,Cu,S |
| Strunz (8:e upplagan) | 1/A.07-10 |
| Hejs CIM Ref. | 1.57 |
| Dana (7:e upplagan) | 1.1.17.1 |
| Molekylvikt | 55.85 |
| Cellalternativ | a = 2,8664Å |
| Antal formelenheter (Z) | 2 |
| Enhet cellvolym | V 23,55 ų |
| Twinning | av (111) |
| Punktgrupp | m3m (4/m 3 2/m) - Hexoktaedrisk |
| Rymdgrupp | Im3m (I4/m 3 2/m) |
| Separation | av (112) |
| Densitet (beräknad) | 7.874 |
| Densitet (uppmätt) | 7.3 - 7.87 |
| Typ | isotropisk |
| Färg i reflekterat ljus | vit |
| Urvalsformulär | Form av kristallina avlagringar: täta korn med oregelbundna slingrande konturer, filmer, dendriter och ibland nuggets. |
| Klasser om taxonomi av Sovjetunionen | Metaller |
Järn är den vanligaste metallen i världen efter aluminium. klot; den utgör cirka 5 % av jordskorpan. Järn finns i form av olika föreningar: oxider, sulfider, silikater. Järn finns i sin fria form i meteoriter; inhemskt järn (ferrit) finns ibland i jordskorpan som en produkt av stelning av magma.
Järn är en del av många mineraler som utgör järnmalmsfyndigheter.
Huvudsakliga järnmalmsmineraler:
Hematit(järnglans, röd järnmalm) - Fe 2 O 3 (upp till 70 % Fe);
Magnetit(magnetisk järnmalm) - Fe 3 O 4 (upp till 72,4 % Fe);
Goethite- FeOOH
Hydrogoethite- FeOOH*nH2O (limonit) - (ca 62% Fe);
Siderit- Fe(CO3) (ca 48,2% Fe);
Pyrit- FeS 2
Järnmalmsfyndigheter bildas under olika geologiska förhållanden; Detta är förknippat med mångfalden av malmsammansättning och förekomstförhållanden. Järnmalm delas in i följande industrityper:
Bruna järnmalmer är malmer av vattenhaltig järnoxid (huvudmineralet är hydrogoetit), 30-55% järn.
Röda järnmalmer, eller hematitmalmer (huvudmineralet är hematit, ibland med magnetit), 51-66% järn.
Magnetiska järnmalmer (huvudmineralet är magnetit), 50-65% järn.
Siderit eller karbonat sedimentära malmer, 30-35% järn.
Silikat sedimentära järnmalmer, 25-40% järn.
Stora reserver av järnmalm finns i Ural, där hela berg (till exempel Magnitnaya, Kachkanar, Vysokaya, etc.) bildas av magnetisk järnmalm. Stora fyndigheter av järnmalm finns nära Kursk, på Kolahalvön, i västra och östra Sibirien, i Långt österut. Det finns rika fyndigheter i Ukraina.
Järn är också ett av de vanligaste grundämnena i naturliga vatten, där dess genomsnittliga halt varierar från 0,01-26 mg/l.
Djurorganismer och växter samlar på sig järn. Vissa typer av alger och bakterier ackumulerar aktivt järn.
I människokroppen varierar järnhalten från 4 till 7 g (i vävnader, blod, inre organ). Järn kommer in i kroppen med mat. En vuxens dagliga behov av järn är 11-30 mg. Grundläggande livsmedel innehåller följande mängder järn (i mcg/100g):
Mjölk - 70
Potatis, grönsaker, frukt - från 600 till 900
II . Teknogena källor för järn som kommer in i miljön.
I områden med metallurgiska anläggningar innehåller fasta utsläpp från 22 000 till 31 000 mg/kg järn.
Jordarna i anslutning till växterna får upp till 31-42 mg/kg järn. Som ett resultat ackumuleras järn i trädgårdsgrödor.
Mycket järn kommer ut i avloppsvatten och slam från industrier: metallurgisk, kemi, ingenjörskonst, metallbearbetning, petrokemi, kemisk-farmaceutisk, färg och lack, textil.
Damm och rök från industriell produktion kan innehålla stora mängder järn i form av aerosoler av järn, dess oxider och malmer.
Damm av järn eller dess oxider bildas vid slipning av metallverktyg, rengöring av delar från rost, rulljärnsplåtar, elektrisk svetsning och andra produktionsprocesser där järn eller dess föreningar förekommer.
Järn kan ansamlas i jordar, vattendrag, luft och levande organismer.
De viktigaste järnmineralerna i naturen genomgår fotokemisk förstörelse, komplexbildning och mikrobiologisk urlakning, som ett resultat av vilket järn övergår från svårlösliga mineraler till vattenkroppar.
Oxidationen av sulfider kan beskrivas i allmänna termer med exemplet med pyrit genom följande mikrobiologiska och kemiska processer:
Som du kan se skapar detta ytterligare en förorening ytvatten komponent - svavelsyra.
Omfattningen av hennes mikrobiologiska utbildning kan bedömas från detta exempel. Pyrit är en vanlig föroreningskomponent i kolavlagringar och dess urlakning leder till försurning av gruvvattnet. Enligt en uppskattning 1932. Cirka 3 miljoner ton H 2 SO 4 kom in i Ohiofloden (USA) med gruvvattnet.
Mikrobiologisk urlakning av järn utförs inte bara på grund av oxidation, utan också under reduktion av oxiderade malmer. Det handlar om mikroorganismer relaterade till olika grupper. I synnerhet utförs reduktionen av Fe 3+ till Fe 2+ av representanter för släktena Bacillus och Pseudomonas, såväl som vissa svampar.
De processer som nämns här, som är utbredda i naturen, förekommer även på soptippen hos gruvföretag och metallurgiska anläggningar som producerar stora mängder avfall (slagg, askar, etc.).
Med regn, översvämning och grundvatten överförs metaller som frigörs från fasta matriser till floder och reservoarer. Järn finns i naturliga vatten i olika tillstånd och former: i verkligt löst form ingår det i bottensediment och heterogena system (suspensioner och kolloider).
Bottensediment av floder och reservoarer fungerar som en järnreservoar. Under vissa förhållanden kan järn frigöras från dem, vilket resulterar i sekundär vattenförorening.
III . Kemiska egenskaper järn, dess huvudföreningar.
Järn är ett grundämne i grupp VIII i det periodiska systemet. Atomnummer 26, atomvikt 55,85 (56). Konfigurationen av atomens yttre elektroner är 3d 6 4s 2.
I naturliga reservoarer, till exempel i Lake Ladoga, i Neva, är järnhalten mindre än 0,3 mg/l. Innan det kommer in i stadens vattenförsörjningsnät, utsätts vatten från reservoarer för filtrering och verkan av koagulanter, som tillsammans med organiska föroreningar också tar bort en del av järnet.
Behandling av vatten med hög järnhalt består av filtrering med hjälp av mekaniska filter (antracit), koagulering (koaguleringsmedel - aluminiumoxid Al 2 (SO 4) 3) och ibland - behandling magnetiska fält(när det gäller magnetiska former av järn).
Förebyggande åtgärder för att säkerställa säkra arbetsförhållanden när arbetare exponeras för järn och dess föreningar bestäms av regulatoriska dokument i förhållande till specifika produktionsförhållanden.
V . Erhålla järn och dess huvudsakliga föreningar, deras praktiska användning.
Av alla utvunna metaller är järn den viktigaste. All modern teknik är förknippad med användningen av järn och dess legeringar. Mängden järn som bryts är cirka 15 gånger större än produktionen av alla andra metaller tillsammans.
Den huvudsakliga industriella metoden för att få järn är dess produktion i form av olika legeringar med kol - gjutjärn och kolstål. Gjutjärn framställs genom masugnsprocessen och stål framställs med öppen härd, omvandlare och elektriska smältprocesser.
De huvudsakliga laddningsmaterialen som är involverade i masugnsprocessen är järnmalm, koks och kalksten, som är nödvändiga för reduktion av järnoxider i malmen med kol och utspädning av smält gjutjärn och slagg.
Luft eller, för att påskynda processen, syre (syreblästring) tillförs masugnen. Kokskol oxideras av syre: C+O 2 =CO 2 ; C+CO2=2CO.
Det resulterande CO- och kokskolet reduceras med järnoxid:
Eftersom dessa reaktioner sker med ett överskott av kol, smälter det reducerade järnet med kolet och producerar gjutjärn med en mycket lägre smältpunkt än rent järn. Gjutjärn (med 4,3 % C) smälter vid 1135 o C och järn vid 1539 o C.
Smält lågsmältande järn och slagg samlas upp i masugnshärden och släpps då och då ut genom speciella öppningar.
Metoder för bearbetning av gjutjärn - öppen härd, omvandlare och elektrisk smältning - reduceras till att avlägsna överskott av kol och skadliga föroreningar (S, P) genom att oxidera dem och till att justera innehållet av legeringselement till ett specificerat värde genom att tillsätta dem under smältning.
Det högsta tillåtna innehållet av skadliga föroreningar och det erforderliga innehållet av legeringselement fastställs för varje stålkvalitet.
Rent järn erhålls i pulverform genom reduktion av dess oxider med väte eller termisk sönderdelning av karbonyl Fe(CO) 5 . Användningen av rent järn är begränsad, eftersom På grund av dess mekaniska egenskaper uppfyller den inte ett antal krav på konstruktionsmaterial. Den är väldigt plastig.
Järn och dess legeringar utgör grunden för modern teknik. Järnlegeringarnas betydelse för tekniken följer av att 95 % av alla metallprodukter är gjutjärn och endast 5 % är legeringar av andra metaller.
Järnföreningar.
bläcksten FeSO4. 7H 2 O erhålls genom att lösa upp stålskrot i 20-30 % svavelsyra:
Järnsulfat är ljusgröna kristaller, mycket lösliga i vatten. Det används för att bekämpa växtskadegörare, vid tillverkning av bläck och mineralfärger, för färgning av tyger och för att behandla avloppsvatten från cyanid.
Vid exponering för järnsulfat bildas alkalier järnhydroxider- Fe(OH)2 och Fe(OH)3.
Dessa hydroxider används som pigment. Naturlig järnhydroxid FeS 2 (pyrit) fungerar som en råvara för framställning av svavelsyra, svavel och järn.
Järnnitrat Fe(NO 3) 3 erhålls genom att behandla järn med salpetersyra. Det används som betningsmedel vid färgning av bomullstyger och som viktmedel för silke.
Järnklorid FeCl 3 bildas genom att värma järn med klor, klorera FeCl 2. Det används som koaguleringsmedel vid vattenrening, som betningsmedel i färgning av tyger och som katalysator vid organisk syntes.
Järnsulfat Fe 2 (SO 4) 3 bildar kristallint hydrat Fe 2 (SO 4) 3. 9H2O (gula kristaller). Erhålls genom att lösa Fe 2 O 3 oxid i svavelsyra. Det används som koaguleringsmedel vid vattenrening, för etsning av metaller och används vid tillverkning av koppar.
Järnoxider erhålls vanligtvis genom inverkan av vattenånga på varmt järn. Naturliga järnoxider fungerar som de viktigaste råvarorna för produktion av metalliskt järn (dess legeringar).
Fe 2 O 3 och dess derivat (ferriter) används i radioelektronik som magnetiska material, inklusive som aktiva ämnen i magnetband.
Fe 3 O 4 fungerar som material för tillverkning av anoder i ett antal elektrokemiska industrier.
Ferriter - när järn(III)oxid smälts samman med natrium- eller kaliumkarbonater bildas ferriter - salter av järn(III)syra HFeO 2 som inte erhålls i fritt tillstånd, till exempel natriumferrit NaFeO 2:
Inom tekniken är ferriter eller ferritiska material produkter av sintring av Fe 2 O 3-pulver och oxider av vissa tvåvärda metaller, till exempel Ni, Zn, Mn.
Ferriter har värdefulla magnetiska egenskaper och högt elektriskt motstånd.
Ferriter används i stor utsträckning inom kommunikationsteknik, datorer, automation och telemekanik.
Järn (VI) föreningar.
Om man värmer stålspån eller Fe 2 O 3 med kaliumnitrat och hydroxid bildas en legering innehållande kaliumferrat K 2 FeO 4 - ett salt av järnsyra H 2 FeO 4, som inte erhålls i fri form.
När legeringen löses i vatten erhålls en rödviolett lösning, från vilken det vattenolösliga bariumferraten BaFeO 4 kan fällas ut genom inverkan av bariumklorid.
Alla ferrater är mycket starka oxidationsmedel, starkare än KMnO 4 .
Järnkarbonyler
Järn bildar flyktiga föreningar med kolmonoxid som kallas järnkarbonyler. Järnpentakarbonyl Fe(CO) 5 är en blekgul vätska, olöslig i vatten, men löslig i många organiska lösningsmedel. Fe(CO) 5 erhålls genom att föra CO över järnpulver vid 150-200 o C och ett tryck på 100 atm. Vid upphettning i vakuum sönderdelas Fe(CO)5 till järn och CO. Detta används för att producera högrent järnpulver - karbonyljärn.
Järnlegeringar är metallegeringar baserade på järn. Innan tidiga XIXårhundraden klassificerades järnlegeringar främst som Fe-C (med inblandningar av Si, Mn, S, P), som kallades stål och gjutjärn. Ökande tekniska krav på metallmaterial, främst i förhållande till deras mekaniska egenskaper, värmebeständighet, korrosionsbeständighet i olika aggressiva miljöer, har lett till skapandet av nya järnlegeringar innehållande Cr, Ni, Si, Mo, W, etc.
För närvarande inkluderar järnlegeringar: kolstål, gjutjärn, legerat stål som innehåller andra element förutom kol och stål med speciella fysikalisk-kemiska och mekaniska egenskaper.
Dessutom används speciella järnlegeringar, kallade ferrolegeringar, för att införa legeringselement i stål.
Inom tekniken kallas järnlegeringar vanligtvis för järnmetaller, och deras framställning kallas järnmetallurgi.
Gjutjärn skiljer sig från stål i sin högre kolhalt och dess egenskaper. Den är ömtålig, men har goda gjutegenskaper. Gjutjärn är billigare än stål. Huvuddelen av gjutjärnet bearbetas till stål.
Element som specifikt införts i stål för att ändra dess egenskaper kallas legeringselement, och stål som innehåller sådana element kallas legerat. De viktigaste legeringselementen inkluderar Cr, Ni, Mn, W, Mo. Värmebeständiga nickelbaserade legeringar (nikrom innehållande nickel och krom och andra) används ofta.
Mynt, smycken och hushållsartiklar är gjorda av koppar-nickellegeringar (cupronickel och andra).
Galvanisering av metaller med nickel ger dem ett vackert utseende.
Lista över använd litteratur:
1. "Koncis kemisk encyklopedi."
(Sovjet Encyclopedia förlag, 1963)
2. M.Kh. Karapetyants, S.I. Drakin - "Allmän och oorganisk kemi"
(Chemistry Publishing House, 1981)
3. N.A. Glinka - "Allmän kemi"
(Chemistry Publishing House, 1975)
4. Katalog "Skadliga kemikalier, oorganiska föreningar av grundämnen i grupperna V-VIII."
(Chemistry Publishing House, 1989)
5. V.A. Isidorov - "Introduktion till kemisk ekotoxikologi"
("Khimizdat", 1999)
Järn är ett viktigt mikroelement för människors hälsa, vars betydelse inte kan överskattas, eftersom det är en del av sjuttio enzymer som skyddar kroppens celler. Denna metall är en viktig biologiskt aktiv substans som har förmågan att snabbt reducera och oxidera.
Järn är involverat i transporten av syre i blodet
Järn i människokroppen är ansvarig för "produktionen" av hemoglobin i blodet, vilket normaliserar näringen av vävnader, system och organ. Detta beror på förbättrad blodcirkulation, som håller kroppen aktiv och frisk.
- Upprätthålla immunförsvaret;
- Ökad fysisk aktivitet;
- Förstärkning av benvävnad;
- Normalisering av blodcirkulationen;
- Upprätthålla sköldkörtelfunktionen;
- Underhåll och återställande av det centrala nervsystemet.
Det finns väldigt lite järn i människokroppen, men trots detta är många funktioner omöjliga utan det. Mineralets huvudroll är produktionen av vita (lymfocyter) och röda (erytrocyter) blod celler. Lymfocyter är ansvariga för immunitet, och röda blodkroppar förser blodet med syre.
Järn kommer in i kroppen direkt från maten. Livsmedelsprodukter av animaliskt ursprung innehåller detta mineral i en lättsmält form. Det finns också vegetabiliska livsmedel som är rika på järn, men kroppen har svårare att ta upp mikroelementet som kommer från sådana källor.
Järn kommer in i matsmältningskanalen, där det utsätts för magsaft, vilket resulterar i dess absorption. Mikroelementet absorberas direkt i tolvfingertarmen, såväl som i den övre delen av tunntarmen. Det är på så sätt som järn kommer in i blodet, där det binder till protein och, tillsammans med blodomloppet, transporteras till de nödvändiga delarna av kroppen.
Vilka livsmedel innehåller järn?
100 gram kött innehåller 2-3 mg järn
Askorbinsyra, sorbitol, fruktos och bärnstenssyra säkerställer bättre upptag av järn i kroppen. Tvärtom, sojaprotein hämmar absorptionen av detta mineral, vilket indikerar behovet av att utesluta produkten från kosten om det finns en brist på järn i kroppen. Te och kaffe innehåller partiklar som negativt påverkar absorptionsprocessen av mikroelementet, så erfarna nutritionister rekommenderar att dricka juice efter måltider, vilket har en gynnsam effekt på absorptionen av järn av cellerna i matsmältningssystemet.
Djurkällor av järn
- Köttprodukter - kalvkött, nötkött, fläsk, kanin, kalkon;
- Biprodukter – lever;
- Skaldjur - skaldjur, sniglar, ostron;
- Fisk - makrill, rosa lax;
- Äggula.
Växtkällor för järn
- Spannmål - hel havregryn, bovete;
- Baljväxter - röda bönor;
- Grönsaker – rödbetor, selleri, blomkål, tomater, pumpa;
- Frukt - äpplen, päron, aprikoser, vindruvor, fikon, persikor;
- Torkad frukt - torkade aprikoser, katrinplommon, dadlar, russin, päron, äpplen;
- Bär - björnbär, blåbär, jordgubbar;
- Valnötter.

Dagliga järnbehov
Av den totala mängden järn som kommer in i kroppen med maten absorberas endast 10 %. Detta beror på att olika produkter som innehåller detta mineral absorberas olika. Med produkter av animaliskt ursprung absorberas mikroelementet mycket snabbare och bättre. Det dagliga järnbehovet bestäms individuellt för varje person, beroende på deras livsstil och ålder.
Dagligt värde för barn
Barnets kropp behöver 5-15 milligram beroende på åldersgrupp, än äldre barn, desto mer mineral behöver den.
Dagligt värde för kvinnor
Kvinnokroppen med hälsosamt sätt liv och rätt näring kräver 20 mg järn. Under graviditeten och tiden efter förlossningen ökar behovet av mineralet och uppgår till 30 milligram per dag.
Dagligt värde för män
Den manliga kroppen behöver 10 till 15 milligram järn. Behovet av detta mikroelement ökar med fysisk aktivitet och missbruk av alkoholhaltiga drycker och rökning.
Brist på järn i kroppen
Järnbrist i människokroppen uppstår i följande fall:
Graviditet, tillväxt och amning kan också leda till järnbrist. Mineralbrist kan utvecklas efter infektionssjukdomar, såväl som med patologiska störningar i tarmfloran.
Frånvaron av köttprodukter i kosten och dominansen av rotfrukter och potatis leder till allvarliga problem i samband med mikroelementbrist.
Konsekvenser av järnbrist
- Utveckling av muskelsvaghet och andnöd;
- Torr hud;
- För tidig uppkomst av rynkor;
- Skört hår och naglar;
- Minnesskada;
- Överdriven irritabilitet;
- Dåsighet;
- Nedsatt koncentrationsförmåga.
Människor som lider av järnbrist i kroppen kännetecknas av blek hud och en tendens att svimma och ofta yrsel.
Överskott av järn i kroppen
Överskott av järn i kroppen leder också till obehagliga konsekvenser, eftersom detta mikroelement har förmågan att ackumuleras i en persons inre organ: hjärtat, levern, bukspottkörteln. Sådan ackumulering kan leda till skador på vävnaderna i inre organ, såväl som störningar av deras fysiologiska funktioner.
Video från Internet
Orsaker till överdosering
- Ökat absorption av järn i tarmen;
- Några ärftliga faktorer;
- Massiv blodtransfusion;
- Okontrollerad användning av läkemedel som innehåller järn.
Preparat som innehåller järn
Järnpreparat är en grupp läkemedel som innehåller salter och komplex av mikroelementföreningar, eller deras kombinationer med andra mineraler. Dessa läkemedel används främst för att förebygga och behandla järnbristanemi.

Läkemedel som innehåller detta mineral bör ordineras av en läkare efter att ha utfört de nödvändiga testerna. Självtillförsel av järn i form av mediciner kan orsaka stor skada på hälsan.
Regler för att ta järntillskott
- Ta med en liten mängd vatten;
- Ta inte oralt med kalciumtillskott, tetracykliner, kloramfenikol eller antacida (almagel, fosfalugel, etc.);
- Öka inte dosen även efter att ha missat en dos.
Biverkningar från att ta järntillskott inkluderar hudrodnad, illamående, minskad aptit, förstoppning eller diarré, tarmkolik och rapningar. I detta fall bör användningen av droger stoppas.
Särskild försiktighet bör iakttas när du tar mediciner av detta mineral. barndom, eftersom en överdos av järn (300 milligram per dag) kan vara dödlig.
För närvarande är de mest populära järnpreparaten följande, som har den mest exakta dosen av mineralet och har ett minimum av biverkningar på kroppen:
- Conferon (Conferon) - Ungersk produktion, som producerar 50 kapslar, som var och en innehåller natriumdioktylsulfosuccinat - 35 mg och järn (II) sulfat - 250 mg (50 milligram elementärt järn). Natrium främjar absorptionen av järn i kroppen och ökar dess terapeutiska effektivitet. Förskrivet för järnbristanemi av olika etiologier.
- Feracryl (Feracrylum) – innehåller ett ofullständigt järnsalt av polyakrylsyror. Finns i form av glasartade, ömtåliga tallrikar av gul eller mörkbrun färg. Svårt att lösa i vatten. Används för att bilda blodproteinproppar. Används som ett lokalt hemostatiskt medel.
- Ferrum Lek är ett järnpreparat för intravenösa och intramuskulära injektioner, tillverkat i Jugoslavien. Doseringen av läkemedlet beräknas individuellt för varje patient.
- Haemostimulinum - ordineras för att stimulera blödning och behandla hypokrom anemi av olika etiologier. Finns i tablettform. Innehåller järnhaltig järnlaktat i mängden 0,246 gram.
Järnhaltiga mineraler flyter under påverkan av reagens - naftenoljesyra, natriumoleat, flytande glas; Nyligen Oxiderad fotogen har använts framgångsrikt. För flotation av manganmalmer används följande reagens: oljesyra, sojabönolja, tvål, lösligt glas, soda.
Det särskiljs från andra järnhaltiga mineraler genom det körsbärsröda strecket kvar på oglaserat porslin. Hematit är ett kemiskt resistent mineral som bildar kraftfulla fyndigheter av järnmalm, som är en värdefull råvara för framställning av gjutjärn och stål. Kända avlagringar av hematitmalmer finns i regionen Kursks magnetiska anomali, i norra Ural, i Ukraina.
Kaolin innehåller alltid fria järnhaltiga mineraler, som har ett brytningsindex på 2 2 - 2 4 och är intensivt färgade, vilket, även om innehållet är obetydligt, ger kaolin en mängd olika nyanser från ljusgult till brunt och rödbrunt. På optiska egenskaper kaolin stort inflytande Titanmineraler har också en effekt, som även i små mängder (högst 1%) kan påverka dess kvalitet.
En hög halt av kvarts, samt järnhaltiga mineraler och andra föroreningar, minskar kvaliteten på brandbeständiga leror och kaoliner, vilket i vissa fall kräver deras anrikning.
När det gäller mineralogisk sammansättning är huvuddelen av slurryn järnhaltiga mineraler: hematit, magnetit, kalciumferrit och pyrit; kvarts, silikater, karbonater (kalk) och spannmålsfragment finns också organiskt ursprung- Cola. Det vanligaste mineralet är hematit. Hematitkorn har en oregelbunden form, deras storlek sträcker sig från fraktioner av en mikron till 0,15 mm, i genomsnitt 0,03 mm. Hematit representeras huvudsakligen av fria korn, sammanväxter av hematit och kvarts är mindre vanliga, liksom små hematitkorn cementerade av ett glasartat ligament (olivin). Kvarvarande magnetit observeras i de största hematitkornen. Det finns inga fria magnetitkorn.
Järnmalmstenar är vanligtvis färgade bruna, gulbruna, grönbruna, beroende på färgen på de järnhaltiga mineral som utgör dem.
De innehåller vanligtvis, jämte de angivna oxiderna av kalium och natrium, olika föroreningar, av vilka de mest skadliga är järnoxider, svavelkis och järnhaltiga mineraler, som ger fältspatarna en gul eller rosa färg. Fältspat ökar emaljens eldfasthet, ökar dess kemiska beständighet och förbättrar dess opacitet i närvaro av flusspat och natriumkiselfluorid. Vid smältning av emalj är det mycket viktig roll Storleken på sparslipningen spelar roll. Ju mer sparren krossas, desto lättare smälter laddningen.
Föroreningar inkluderar även kiseldioxid i form av kvarts och opal, mindre vanligt kalcedon, titandioxid i form av rutil och ilmenit, järn i form av olika järnhaltiga mineraler: limonit, hematit, siderit, etc. Vissa kaoliner innehåller gibbsit- och diaspormineraler , som ett resultat av vilket De visar ett ökat innehåll av aluminiumoxid.
Dessutom tillsätts speciella viktmedel till lerlösningen för att få dess densitet till 1 6 - 2 0 kg / dm3 istället för 1 2 för en vanlig lösning. Järnhaltiga mineraler (magnetit, hematit), baryt och masugnsdammkoncentrat används som viktningsmedel. En sådan lösning med viktningsmedel används om trycket i brunnen är onormalt högt eller i bottenhålszonen börjar lösningen att bli mättad med gas eller olja som bryter in i den.
Källan till järn är kristallina bergarter som innehåller många järnhaltiga mineraler. Under vittringsprocesser förvandlas järn till hydroxid och transporteras med vatten i form av mekanisk suspension och kolloider av järnhydroxid. Partiell överföring sker i form av järnsulfater och bikarbonater. Järnet som förs på detta sätt fördelas i reservoarer enligt lagarna för mekanisk differentiering i enlighet med bassängens hydrodynamik. Eftersom suspensionspartiklar och kolloider är små i storlek, observeras de största (clark) mängderna järn i leriga; nederbörd
Wollastonit finns främst i marmorerade kalkstenar eller kalkhaltiga kristallina skiffer. Som föroreningar åtföljs det av kvarts, järnhaltiga mineraler, kalkhaltiga granater, diopsid, vesuvian och andra mineraler.
Det mest bekväma för att identifiera förhållanden eller fluktuationer i redoxsituationen är järnhaltiga mineraler som är utbredda i naturen, och för att identifiera miljöns reaktion, mineraler från lergruppen och karbonatmineraler.
Enligt en sammanfattning sammanställd av E.M. Bonstedt klassificeras nefelinavlagringar i Sovjetunionen enligt följande. De enorma ansamlingarna av Khibiny-tundran här är av obestridlig industriell betydelse: 1) nefelinsand, tvättad och till stor del rensad från järnhaltiga mineraler, produkter från maskinteknik. Imandra mellan stationen. Khibiny och Imandra, som utgör de stora och små sandiga navolokerna; enligt P. A. Borisovs beräkningar är den totala reserven av nefelinsand upp till 900 000 ton; de innehåller upp till 60 - 70% nefelin; kemisk Separata länkar i denna båge är de kraftfulla intrången av Kuelspor och Porisom-chorr. Den mineralogiska sammansättningen av dessa bergarter ges i tabell. 3 (enligt V.
Egenskaper för lerråvaror enligt innehållet av fina fraktioner (enligt GOST 9169 - 75.
Baserat på storleken på grovkorniga inneslutningar delas leror in i grupper med små inneslutningar (mindre än 1 mm), medelstora - från 1 till 5 mm, stora - över 5 mm. Baserat på typen av stora inneslutningar delas leror in i grupper med inneslutningar av stenfragment (granit, skiffer, kvartsiter, etc.); järnhaltiga mineraler; gips; karbonater (kalcium, dolomit, etc.); organiska restprodukter och kol. Beroende på innehållet av fri kvarts delas lerråvaror in i grupper med låg (upp till 10%), medium (över 10 till 25%) och hög (över 25%) kvartshalt.
Järnhaltiga bergarter inkluderar järnmalmer av sedimentärt ursprung, oxid, karbonat, silikat och olika järnhaltiga formationer - orsteins, orzands, såväl som sandplacerare rika på järnhaltiga mineraler.
Selektivitetskoefficienter (Ett par tungmetallkatjoner - Ca2 (enligt B.S. Gorbatov. Vid oxidativ vittring och jordbildning bildas och ackumuleras järn(III)mineraler i biosfären, främst oxider och hydroxider, svagt lösliga och geokemiskt relativt inerta. Många järn (II) mineraler finns i jordar ) och järn (III), inklusive oxider: hematit Fe2O3, magnetit FeO Fe2O3; maghemite Fe2O3; hydroxider: goetite FeOOH, limonit 2Fe2O3 ZH2O; sulfider; sura järnhaltiga mineraler: jarosit (OH)Fe6 12 (SO4) 4l, feronatrit [Na3Fe (SO4) 3 3H2O], fosfater, silikater, järnarsenater, organiska järnhaltiga föreningar, amorfa fällningar av hydroxider.
Under det proterozoiska stadiet, som varade i 1 - 15 miljarder år, var vulkanaktiviteten mindre intensiv, och olika sediment ackumulerades i haven och haven. I vissa proterozoiska vattenbassänger utvecklades de intensivt olika organismer(till exempel järnutfällande bakterier, alger etc.), på grund av vilka sedimenten berikades med järn eller karbonater. Det är därför järnhaltiga mineraler (malmer och järnhaltiga kvartsiter från Kursks magnetiska anomali, Kanada, etc.), tjocka skikt av kalksten, ofta alger, och dolomiter, och ibland lager av shungiter - en prototyp av framtida kol - är ganska vanliga i proterozoikum insättningar. I många delar av världen sänktes proterozoiska sediment ner till stora djup, deformerades kraftigt och penetrerades av het magma, som ett resultat av vilket de förändrades kraftigt och förvandlades till gnejser, kvartsiter och andra metamorfa bergarter.
Konventionell mekanisk förädling ger inte högkvalitativa koncentrat från sådana produkter i kombination med tillfredsställande återvinning. Även om det är osannolikt att alla möjligheter för mekanisk anrikning av järnhaltiga mineralblandningar är uttömda, bör det antas att lösningen på denna fråga är mycket komplex och kommer att kräva långsiktig forskning om fundamentalt nya metoder baserade på subtil användning av skillnader i de fysikaliska och fysikalisk-kemiska egenskaperna hos järnhaltiga mineraler. Under dessa förhållanden blir metoder för selektiv upplösning av järnhaltiga mineraler samtidigt som värdefulla sällsynta metallmineraler bevaras i en olöslig rest särskilt viktiga.
I form av slumpmässiga föroreningar kommer metalliskt järn in i malmen vid borrning eller provtagning och malning av ett prov. Om järnmalmen inte innehåller magnetit, maghemit, pyrrotit eller andra mineraler som har magnetiska egenskaper kan metalliskt järn avlägsnas från malmen med hjälp av en magnet. Man bör komma ihåg att ett antal järnhaltiga mineraler, såsom hematit (martit och järnglans), goetit, hydrogoetite, hydrohematit och några andra, har förmågan att magnetiseras i ett elektromagnetiskt fält.
Uzyanbash, manganmineralisering av liknande typ upptäcktes också. Här, på östra sidan av samma motorväg, s. I Sermenevo-Askarovo är en lerig krossad eluvial vittringsskorpa exponerad, förmodligen över kvartssiltstenar och kvartsit-sandstenar. Lösa sediment har en ljus gulbrun färg, vilket indikerar ett ökat innehåll av järnhaltiga mineraler i de ursprungliga bergarterna. I de eluviala fragmenten av värdsedimenten finns ofta avlagringar av manganoxider och ibland små bitar av ådspridad till fast manganmalm.
Naturligtvis kan sanden även innehålla andra steniga ämnen som antingen är oförändrade av vatten eller svåra att förändra, men eftersom dessa senare är mer eller mindre föremål för förändring under långvarig inverkan av vatten, är det inte ovanligt att hitta sand som endast innehåller nästan ren kvarts. Vanlig sand har på grund av inblandning av främmande mineral en gul eller rödbrun färg, beroende på järnhaltiga mineraler och järnhaltig lera. Den renaste sanden, eller den s. k. kvartssanden, påträffas dock ganska sällan och kännetecknas av sin färglöshet och att den vid vattenskakning ej framkallar grumlighet, som tyder på en inblandning av lera; när det smälts samman med baser producerar det färglöst glas, vilket är anledningen till att det är ett värdefullt material för glasproduktion.
Nefelin är en betydande del av dessa bergarter; Vid framställning av apatitkoncentrat erhålls avfall som innehåller 70 - 75 % nefelin. Urtite och yolit vener finns också i de mindre utforskade Lovozero tundras; Vennefelinstenar finns också vid Vita havets kust, på Turyhalvön, i Tjeckiska bukten, etc. Ett annat område för ansamling av nefelinstenar är södra Ural, där nefelinsyeniter-miaskiter bildar en meridional remsa ca. . Ilmen Mountains, Cherry Mountains, etc. I sammansättningen av miassiter är nefelin endast 20 - 25% med ett ganska högt innehåll av färgade järnhaltiga mineraler; därför praktiskt
Detta kan endast fastställas genom mineralogisk analys, genom direkt studie av autentiska mineral i tunna sektioner, vilket gör det möjligt att identifiera hela förloppet av autentisk mineralbildning och därigenom fastställa förändringar i geokemiska förhållanden vid olika stadier av litogenesen. Kemisk analysdata bör därför endast tolkas i samband med data från mineralogiska och petrografiska studier. Med hänsyn till detta, och även genom att använda en enorm mängd faktamaterial om olje- och gasregionerna i Uzbekistan, föreslog vi (A. M. Akramkhodzhaev och Kh. Kh. Avazkhodzhaev) att man skulle särskilja sex typer av geokemiska miljöer, bestämda av förhållandet mellan reaktiva former av järn, syngenetiska och diagenetiska järnmineraler och innehållet av resterande OM .
Det finns dock fall då gas- eller oljetrycket är mycket större än det hydrostatiska trycket för ett givet djup. För att förhindra blåsning används i dessa fall viktade lerlösningar. För att göra detta, tillsätt finmalda ämnen med hög densitet till lösningen. Sådana ämnen inkluderar järnmineralerna magnetit och hematit, masugnsdammkoncentrat och baryt.
Samtidigt, genom att jämföra egenskaperna hos magnet- och gravitationsfälten, kan man se att det indikerade området kännetecknas av intensiva negativa gravitationsavvikelser, och regionen i South Absheron-depressionen kännetecknas av ett regionalt, gravitationsmässigt, negativt extremum. Allt detta tycks inte tyda på utvecklingen av täta magnetiskt aktiva kroppar här vid basen av den sedimentära sektionen och kräver en sökning efter en annan förklaring till det svagt positiva fältet i södra Kaspiska havet. Som sådan kan påverkan av det ökade innehållet av magnetiskt aktiva, främst järnhaltiga mineraler i sammansättningen av den okonsoliderade, sandig-leriga delen av kenozoikum i det södra Kaspiska bassängen övervägas. Indirekta tecken Detta beror på de geokemiska egenskaperna hos moderna bottensediment, som visar ett ökat innehåll av plastmagnetit och titanomagnetit i sand och järnhaltiga mineraler i lerbergarter, samt en ökad halt av järn i askrester från oljor från södra Kaspiska havet, en del av som kan fångas upp av vätska från värdstenarna.
Förekomsten av metalliskt järn i järnmalm är ett mycket sällsynt fenomen. I form av naturligt järn (pallasit) finns det i vissa magmatiska avlagringar. Som en förorening kommer metalliskt järn in i malmen under borrning eller provtagning och malning av ett prov. Om järnmalmen inte innehåller magnetit, maghemit, pyrrotit eller andra mineraler som har magnetiska egenskaper kan metalliskt järn avlägsnas från malmen med hjälp av en magnet. Man bör komma ihåg att ett antal järnhaltiga mineraler, såsom hematit (martit och järnglans), goetit, hydrogoetite, hydrohematit och några andra, magnetiseras i ett elektromagnetiskt fält. I sådana fall kan metalliskt järn inte avlägsnas med en magnet och måste bestämmas tillsammans med FeO och Fc20s, enligt nedan.
Wehler framförde en serie viktig forskning, tillägnad titan, detta mycket vanliga element i jordskorpan, vars enorma praktiska betydelse endast manifesteras i vår tid. Upptäckten av titan förknippas i första hand med namnet på den utmärkte mineralanalytikern V. Gregor, som 1789 fastställde att rutilen innehöll ett tidigare okänt grundämne. Klashroth 1795 fann att vissa järnhaltiga mineraler innehåller nytt land- titanoxid. Namnet på elementet gavs av Klaproth.
Nästa steg i prospekteringsarbetet, fokuserat främst på sökandet efter djupa olje- och gasfyndigheter i de södra, centrala och norra zonerna, ledde till upptäckten av Niyazbekfältet och Ter-gachi. Sökandet efter djupa och ultradjupa ansamlingar av olja och gas är förknippat med de viktigaste utsikterna för olje- och gaspotentialen i Ferganabassängen. FEREYDUN-MARJAN OLJEFÄLT - beläget i Persiska viken på gränsen till Saudiarabien och Iran, nordost om Zuluffältet, på stupet av den centralarabiska landhöjningen och begränsat till en kupol som mäter 24 X X 24 km. Sandstenarna i Burgan-formationen är också oljeförande. FERROLIT - kemogene bergarter, 50% eller mer sammansatt av olika järnhaltiga mineraler.
Nästa steg i prospekteringsarbetet, huvudsakligen fokuserat på att söka efter djupa olje- och gasfyndigheter i de södra, centrala och norra zonerna, ledde till upptäckten av Niyazbekfältet och Ter-gachi. Sökandet efter djupa och ultradjupa ansamlingar av olja och gas är förknippat med de främsta utsikterna för olje- och gaspotentialen i Ferganabassängen. FEREYDUN-MARJAN OLJEFÄLT - beläget i Persiska viken på gränsen till Saudiarabien och Iran, nordost om Zuluffältet, på stupet av den centralarabiska landhöjningen och begränsat till en kupol som mäter 24 X X 24 km. Sandstenarna i Burgan-formationen är också oljeförande. FERROLIT - - kemogene bergarter, 50 % eller mer sammansatta av olika järnhaltiga mineraler.
Serpentiniter har nätformiga och loopade strukturer. I det första fallet består de av kilformad y-ödla, som lätt diagnostiseras genom negativ förlängning. Mellanrummen mellan y-ödlakilarna är fyllda med isotrop serpofyt. Den loopade strukturen är karakteristisk för a-ödlor. Serpentiniter innehåller också krysotil. Det fyller vanligtvis sprickor och är en senare formation. Enligt A.A. Alekseeva / 1976 /, serpentiniterna i Kiryabinsky-massivet är sammansatta av mer järnhaltiga mineraler jämfört med liknande bergarter i Birsa-komplexet.
Omräkning av kemiska analyser av flogopit från flogopitavlagringar visade att en ökning av halten av inte bara FeO, utan även Fe2O3 åtföljs av en minskning av magnesiumoxidhalten och en ökning av aluminiumoxidhalten (Korzhinsky, 1945b s. Fe, järn och oxid, är isomorft med Mg, eftersom i detta fall sammansättningsfälten för flogopit och klinopyroxen visar sig vara de smalaste. Om man antar att ett järnhaltigt järn är isomorft med magnesium, sprids sammansättningspunkterna för flogopit i i större utsträckning. Vissa författare har föreslagit att från början allt järn från ferromagnesiska glimmer, såväl som hornblende och vissa pyroxener, kunde ha varit i järnhaltigt tillstånd, isomorft med magnesium, med efterföljande oxidation av en del av järnet när temperaturen sjönk. Fe/Mg i gruppen (Mg Fe) leder till en förändring i sammansättningen av dessa mineraler i förhållande till andra komponenter; i synnerhet leder det i flogopit till en ökning av aluminiumoxidhalten. Detta berövar oss möjligheten till exakt representation på ett diagram (Fig. För flogopitavlagringar som förekommer bland mer järnhaltiga bergarter, till exempel bland pyroxenamfiboliter, är inte bara mer järnhaltiga mineraler karakteristiska, utan även mineralernas paragenetiska förhållanden förändras. Nämligen , istället för associationen av diopsid skapolit phlogopite (Fig.
Geokemi av järn
elev i årskurs 9 "B"
Raevsky Georgy
Järn är inte bara den viktigaste metallen i naturen omkring oss, det är grunden för kultur och industri, det är ett krigsvapen och fredligt arbete. Och det är svårt att hitta ett annat element i hela det periodiska systemet som skulle vara så kopplat till mänsklighetens tidigare, nuvarande och framtida öden.
Akademiker Alexander Evgenievich Fersman, framstående sovjetisk geokemist, mineralog, geograf och resenär
Vad är geokemi?
Den romerske lärde författaren, författaren till Natural History, Plinius den äldre, skrev: ”Järnmalmsgruvor förser människan med det mest utmärkta redskapet. För med detta instrument skär vi genom jorden, odlar fruktbara trädgårdar och beskär vilda vinstockar med druvor, tvingar dem att växa unga varje år. Med det här verktyget bygger vi hus, krossar stenar och använder järn för alla sådana behov.”
Mineraler, inklusive järn, värderades inte bara i början av den kristna eran, under Plinius tid. I vårt århundrade, otänkbart utan vetenskaplig och teknisk utveckling och utvecklad industri, har deras betydelse ökat ännu mer. Men för att mänskligheten ska ta emot de nödvändiga elementen i tillräckliga mängder måste de ständigt utvinnas. Och för detta behöver du känna till distributionsmönstren kemiska grundämnen På jorden.
Studiet av dessa mönster ockuperas av olika vetenskaper, bland vilka den ledande platsen är upptagen av geokemi - vetenskapen om jordens kemiska sammansättning, lagarna för distribution av element och deras isotoper och processerna för bildning av stenar, jordar och naturliga vatten. (Om någon är intresserad, vetenskapen om kosmokemi är engagerad i samma forskning i utomjordiskt utrymme). Eftersom kemiska grundämnen finns i jordskorpan i form av malmer och mineraler, är geokemi å ena sidan kemins syster, å andra sidan är den nära besläktad med geologi. Och ett av geologins huvudområden är studiet av fördelningen av mineraler i jordskorpan. Därför betraktas geokemi ofta som ett slags hybridvetenskapligt fält som uppstod på gränsen mellan geologi och kemi. Så följande "ekvation" kommer att vara delvis sann: "geokemi = geologi + kemi" - men bara delvis.
Termen "geokemi" dök upp under den sista fjärdedelen av 1800-talet. Förmodligen introducerades den i vetenskapligt bruk av en av de första professionella geokemisterna - den amerikanske vetenskapsmannen Frank Clark (1847-1931), som kallas geokemins fader.
Den enastående ryska vetenskapsmannen V.I. Vernadsky anses med rätta vara en av grundarna av modern geokemi. 1927 dechiffrerade han innehållet i denna vetenskap på följande sätt: "Geokemi studerar kemiska element, det vill säga atomer i jordskorpan och, så långt som möjligt, hela planeten. Hon studerar deras historia, deras fördelning och rörelse i rum-tid, deras genetiska relationer på vår planet.”
För närvarande är den vanligaste synen på ämnet och innehållet i geokemi följande: modern geokemi studerar fördelningen och innehållet av kemiska grundämnen i mineraler, malmer, stenar, jordar, vatten och den atmosfäriska cirkulationen av grundämnen i naturen baserat på egenskaperna hos deras atomer och joner.
Järn är ett av de vanligaste grundämnena i solsystemet, särskilt på de jordiska planeterna, särskilt på jorden. En betydande del av jordplanets järn finns i kärnorna på planeter, inklusive jorden, där dess innehåll når 90%. Järnhalten i jordskorpan är från 4 till 5 % och i manteln cirka 12 %. Av metallerna är järn näst efter aluminium i överflöd i barken. Samtidigt finns cirka 86 % av allt järn i kärnan och 14 % i manteln.
Järnhalten ökar markant i mafiska magmatiska bergarter, där det är förknippat med pyroxen, amfibol, olivin och biotit. Järn ansamlas i industriella koncentrationer under nästan alla exogena och endogena processer som sker i jordskorpan. Havsvatten innehåller järn i mycket små mängder, 0,002 - 0,02 mg/l. I flodvatten är den något högre – 2 mg/l.
Järn spelar en stor roll i biosfären, eftersom järnatomen är en del av hemoglobin, proteinet i röda blodkroppar i högre organismer. Hemoglobin är involverat i leveransen av syre till vävnader och celler.
Man tror att järn, tillsammans med nickel, kobolt och syre (enligt en annan teori - väte) är en del av jordens kärna. Trycket i jordens mitt är kolossalt (cirka 3 miljoner atmosfärer), och egenskaperna hos dessa element, inklusive järn, bör bli ovanliga. Forskare tror att med sådan kompression blir väte en metall, och den elektroniska strukturen hos atomer av järn och andra metaller (främst de yttre elektronskalen) kan förändras mycket. Men även om science fiction-författare redan har beskrivit resan till jordens centrum många gånger, kan vi inte direkt studera sammansättningen av jordens kärna: geokemister bedömer den på grundval av indirekta data.
Järns geokemiska egenskaper
Den viktigaste geokemiska egenskapen hos järn är närvaron av flera oxidationstillstånd. Järn i neutral form - metalliskt - utgör jordens kärna, finns möjligen i manteln och finns mycket sällan i jordskorpan. Järnhaltigt järn FeO är den huvudsakliga formen av järn som finns i manteln och skorpan. Järnoxid Fe2O3 är karakteristisk för de översta, mest oxiderade delarna av jordskorpan, i synnerhet sedimentära bergarter.
När det gäller kristallkemiska egenskaper ligger Fe2+-jonen nära Mg2+- och Ca2+-jonerna - andra huvudelement som utgör en betydande del av alla jordiska bergarter. På grund av kristallkemisk likhet ersätter järn magnesium och, delvis, kalcium i många silikater. I detta fall ökar vanligtvis järnhalten i mineraler med varierande sammansättning med sjunkande temperatur.
Järnmineraler
Järn är ganska utbrett i jordskorpan - det står för cirka 4,1% av massan av jordskorpan (4:e plats bland alla element, 2:a bland metaller). I manteln och skorpan är järn koncentrerat huvudsakligen i silikater, medan dess innehåll är betydande i basiska och ultrabasiska bergarter, och lågt i sura och mellanliggande bergarter.
Ett stort antal malmer och mineraler som innehåller järn är kända. Malmer är naturliga mineraler som innehåller järn i sådana mängder och föreningar att industriell utvinning av metallen från dem är ekonomiskt genomförbar. Järnhalten i industrimalmer varierar kraftigt – från 16 till 70 %. Beroende på den kemiska sammansättningen används järnmalmer för att smälta gjutjärn i naturlig form eller, om de innehåller mindre än 50 % Fe, efter anrikning. De flesta järnmalmer används för smältning av gjutjärn, stål och ferrolegeringar. I relativt små mängder används de som naturliga färger (ockra) och viktningsmedel för att borra lerlösningar.
Av största praktiska betydelse är röd järnmalm (hematit, Fe2O3; innehåller upp till 70 % Fe), magnetisk järnmalm (magnetit, FeO.Fe2O3, Fe3O4; innehåller 72,4 % Fe), brun järnmalm eller limonit (goetit och hydrogoetit och hydrogoetit). FeOOH respektive FeOOH nH2O). Goetit och hydrogoetit finns oftast i vittringsskorpan och bildar så kallade "järnhattar", vars tjocklek når flera hundra meter. De kan också vara av sedimentärt ursprung och falla ur kolloidala lösningar i sjöar eller kustområden i haven. I det här fallet bildas oolitiska, eller baljväxter, järnmalmer. De innehåller ofta vivianit Fe(3PO4)2·8H2O, som har formen av svarta långsträckta kristaller och radiella aggregat.
Järnsulfider är också utbredda i naturen - pyrit FeS2 (svavel eller järnkis) och pyrrotit. De är inte järnmalm - pyrit används för att göra svavelsyra, och pyrrotit innehåller ofta nickel och kobolt.
Andra vanliga järnmineraler:
· Siderite - FeCO3 - innehåller cirka 35% järn. Den har en gulvit (med en grå eller brun nyans om den är smutsig) färg.
· Marcasite - FeS2 - innehåller 46,6% järn. Det förekommer i form av gula, mässingsliknande, bipyramidala rombiska kristaller.
· Löllingit - FeAs2 - innehåller 27,2% järn och förekommer i form av silvervita bipyramidala rombiska kristaller.
· Mispickel - FeAsS - innehåller 34,3% järn. Det förekommer i form av vita monokliniska prismor.
· Melantherite - FeSO4·7H2O - är mindre vanligt i naturen och är gröna (eller grå på grund av föroreningar) monoklina kristaller med en glasig lyster och spröda.
· Vivianit - Fe3(PO4)2·8H2O - förekommer i form av blågrå eller gröngrå monokliniska kristaller.
Jordskorpan innehåller även andra, mindre vanliga järnmineraler, såsom:
Huvudsakliga järnmalmsfyndigheter
De viktigaste järnfyndigheterna finns i Australien, Brasilien, Venezuela, Indien, Kanada, Liberia, Ryssland, USA, Frankrike, Sverige.
Ryssland är en av de första i världen när det gäller järnmalmsreserver.
De viktigaste fyndigheterna av järnmalm på den geologiska kartan över världen
Intressant geokemiskt faktum:
Mycket få grundämnen förekommer i fri form i naturen. I denna form kallas de infödda. Metaller och de flesta icke-metaller kombineras med andra grundämnen, särskilt syre, mycket lätt. Därför finns de i jordskorpan nästan alltid i en bunden form, som en del av olika föreningar. Järn är ett mycket aktivt element som lätt oxideras, särskilt i närvaro av fukt. Däremot förekommer naturligt järn i naturen. Detta är ett helt exceptionellt fall, eftersom järn i sin ursprungliga form kommer in i jordskorpan som en del av meteoriter.
Och här är vad akademiker Fersman säger i en populär bok om järns geokemi:
"Järn tillhör de viktigaste metallerna i universum. Vi ser hans repliker hos alla kosmiska kroppar, de gnistrar för oss i heta stjärnors atmosfär, vi ser stormiga järnatomer, rastlösa på solytan, faller de till oss årligen på jorden i form av fint kosmiskt stoft, i form av järnmeteoriter. I Arizona, i Sydafrika, i vår Podkamennaya Tunguska-bassäng föll enorma massor av inhemskt järn, denna universums viktigaste metall. Geofysiker hävdar att hela jordens centrum består av en massa nickeljärn, och att vår jordskorpa är i samma skala som de glasartade slagger som strömmar från en masugn under smältningen av tackjärn.
...Geokemister avslöjar för oss järnets historia. De säger att till och med jordskorpan består av 4,2 % järn, och att av metallerna är det bara aluminium som är rikligare i naturen omkring oss än järn. Vi vet att det är en del av de smälta massorna som i form av olivin- och basaltbergarter stelnar i djupet som de tyngsta och mest urbergarter. järn geokemi mineralfyndighet
Vi vet att relativt lite järn finns kvar i granitbergarter; deras ljusa färger - vit, rosa, grön - indikerar järn. Men på jordens yta samlar komplexa kemiska reaktioner fortfarande enorma reserver av järnmalm. Några av dem bildas i subtropikerna, där perioder av tropiska regn ger vika för ljusa soliga dagar av varm sommar, där allt lösligt tvättas ut ur klipporna och stora ansamlingar bildas - skorpor av järn- och aluminiummalm.
Vi vet hur till botten av sjöar nordliga länder Till exempel, i vårt Karelen, tar turbulenta vatten som innehåller organiskt material till våren enorma mängder järn från olika bergarter; På botten av sjöar, där vatten rinner, deponeras ärter eller hela järnkonkreter med deltagande av speciella järnbakterier... Så, i träsk, havets djup, under en lång tidsperiod geologisk historia ansamlingar av järnmalm har bildats på vår jord; och det råder ingen tvekan om att djur- och växtlivet i ett antal fall haft sitt inflytande på bildandet av dessa avlagringar.
Så här bildades stora Kerch-avlagringar; Det är så, med all sannolikhet, de enorma reserverna av järnmalm i Krivoy Rog och Kursks magnetiska anomali bildades.
Malmerna av dessa två sista fyndigheter avsattes så länge sedan av forntida hav, att den heta andedräkten från djupen lyckades förändra deras struktur, och i stället för bruna järnmalmer, som i Kerch, ser vi här förändrade svartmalmer, bestående av av järnglans (hematit, eller röd järnmalm) och magnetisk järnmalm.
Järnvandringen stannar inte på jordens yta. Det är sant att mycket lite av det ackumuleras i havsvatten; och de säger med rätta att detta vatten nästan inte innehåller något järn. Men under speciella exceptionella förhållanden, även i havet, i grunda vikar, avsätts järnhaltiga sediment och hela järnmalmsfyndigheter, vilka också finns i ett antal forntida marina fyndigheter. Så här bildades våra berömda järnmalmsfyndigheter i Ukraina nära Khopr, Kerch och Ayati. Men på jordens yta - i bäckar, floder, sjöar, träsk - vandrar järn överallt; och växter finner alltid detta viktiga kemiska element för sig själva, utan vilket växtliv är omöjligt. Försök att beröva en kruka med blommor av järn, och du kommer att se att blommorna snart kommer att tappa färg och lukt, löven blir gula och börjar torka ut...
... Alltså, i en växt, i en levande organism är järnets kretslopp på jorden fullbordat, och röda blodkroppar i mänskligt blod är ett av de sista stadierna i denna metalls resa, utan vilken det varken finns liv eller fredligt arbete.”
Framtiden för järn
Järnåldern – en era som började i mänsklighetens primitiva historia, då järnmetallurgi och tillverkning av järnverktyg uppstod – fortsätter. Ungefär alla nittio av alla metaller och legeringar som används av mänskligheten är gjorda av järn. Järn smälts i världen ungefär 50 gånger mer än aluminium, för att inte tala om andra metaller. Plast? Men i vår tid utför de oftast andra funktioner i olika strukturer, och om de i enlighet med tradition försöker introducera dem till rangen "oersättliga substitut", så ersätter de oftast icke-järnmetaller, inte järnhaltiga. . Bara några få procent av plasten vi förbrukar ersätter stål.
Järnbaserade legeringar är universella, tekniskt avancerade, tillgängliga och billiga i bulk. Råvarubas Denna metall orsakar inte heller oro: redan utforskade reserver av järnmalm är tillräckligt för människor. Dessutom är forskare övertygade om att de upptäckter som kommer att göras inom geokemi av järn (och i framtiden - järns kosmokemi) kommer att ge mänskligheten nya källor till detta oersättliga element. Forskning inom detta område av geokemi är nödvändig eftersom järn utan att överdriva kan kallas grunden för vår civilisation.
Litteratur
1) Wikipedia, artikel "Järn"
2) Stora sovjetiska encyklopedin, artikel "Järnmalm"
(http://bse.sci-lib.com/article039128.html).
Järnmalm började brytas av människor för många århundraden sedan. Redan då blev fördelarna med att använda järn uppenbara.
Att hitta mineralformationer som innehåller järn är ganska lätt, eftersom detta element utgör cirka fem procent av jordskorpan. Sammantaget är järn det fjärde vanligaste grundämnet i naturen.
Det är omöjligt att hitta det i sin rena form, järn finns i vissa mängder i många typer av stenar. Järnmalm har den högsta järnhalten, vars utvinning av metall är den mest ekonomiskt lönsamma. Mängden järn den innehåller beror på dess ursprung, vars normala andel är cirka 15 %.
Kemisk sammansättning
Järnmalmens egenskaper, dess värde och egenskaper beror direkt på dess kemisk sammansättning. Järnmalm kan innehålla olika mängder järn och andra föroreningar. Beroende på detta finns det flera typer:
- mycket rik, när järnhalten i malmerna överstiger 65 %;
- rik, andelen järn i vilken varierar från 60 % till 65 %;
- genomsnitt, från 45 % och över;
- dålig, där andelen användbara element inte överstiger 45%.
Ju fler biprodukter det finns i järnmalmen, desto mer energi behövs för att bearbeta den, och desto mindre effektiv är produktionen av färdiga produkter.
Sammansättningen av en bergart kan vara en kombination av olika mineraler, gråberg och andra biprodukter, vars förhållande beror på dess avlagring.
Magnetiska malmer kännetecknas av att de är baserade på en oxid som har magnetiska egenskaper, men vid kraftig uppvärmning går de förlorade. Mängden av denna typ av sten i naturen är begränsad, men järnhalten i den kan vara lika bra som röd järnmalm. Externt ser det ut som solida svartblåa kristaller.
Sparjärnmalm är en malmbergart baserad på siderit. Mycket ofta innehåller den en betydande mängd lera. Denna typ av sten är relativt svår att hitta i naturen, vilket i kombination med dess låga järnhalt gör att den sällan används. Därför är det omöjligt att klassificera dem som industrityper av malmer.
Förutom oxider innehåller naturen andra malmer baserade på silikater och karbonater. Mängden järnhalt i en bergart är mycket viktig för dess industriella användning, men också viktig är närvaron av nyttiga biämnen som nickel, magnesium och molybden.
Ansökningar
Tillämpningsområdet för järnmalm är nästan helt begränsat till metallurgi. Det används främst för att smälta gjutjärn, som bryts med öppen spis eller omvandlarugnar. Idag används gjutjärn inom olika sfärer av mänsklig verksamhet, inklusive i de flesta typer av industriell produktion.
Olika järnbaserade legeringar används inte mindre - stål är det mest använda på grund av dess styrka och anti-korrosionsegenskaper.
Gjutjärn, stål och olika andra järnlegeringar används i:
- Maskinteknik, för tillverkning av olika maskiner och apparater.
- Bilindustri, för tillverkning av motorer, hus, ramar, samt andra komponenter och delar.
- Militär- och missilindustrin, vid tillverkning av specialutrustning, vapen och missiler.
- Konstruktion, som förstärkningselement eller konstruktion av bärande konstruktioner.
- Lätt och livsmedelsindustri, som containrar, produktionslinjer, olika enheter och enheter.
- Gruvindustrin, som speciella maskiner och utrustning.
Järnmalmsfyndigheter
Världens järnmalmsreserver är begränsade i kvantitet och läge. Territorier för ackumulering av malmreserver kallas fyndigheter. Idag är järnmalmsfyndigheter indelade i:
- Endogen. De kännetecknas av en speciell placering i jordskorpan, vanligtvis i form av titanomagnetitmalmer. Formerna och placeringen av sådana inneslutningar varierar, de kan vara i form av linser, lager belägna i jordskorpan i form av avlagringar, vulkaniska avlagringar, i form av olika vener och andra oregelbundna former.
- Exogen. Denna typ inkluderar avlagringar av bruna järnmalmer och andra sedimentära bergarter.
- Metamorfogena. Som inkluderar kvartsitavlagringar.
Avlagringar av sådana malmer kan hittas över hela vår planet. Det största antalet fyndigheter är koncentrerat till de postsovjetiska republikernas territorium. Speciellt Ukraina, Ryssland och Kazakstan.
Länder som Brasilien, Kanada, Australien, USA, Indien och Sydafrika har stora järnreserver. Samtidigt har nästan varje land på jorden sina egna utvecklade fyndigheter, i händelse av brist på dessa importeras rasen från andra länder.
Järnmalmsutnyttjande
Det finns som sagt flera typer av malmer. Rika kan bearbetas direkt efter utvinning från jordskorpan, andra behöver berikas. Utöver förädlingsprocessen omfattar malmförädlingen flera steg, såsom sortering, krossning, separering och agglomerering.
Idag finns det flera huvudmetoder för anrikning:
- Spolning.
Den används för att rensa malmer från biprodukter i form av lera eller sand, som tvättas ut med högtrycksvattenstrålar. Denna operation gör det möjligt att öka mängden järnhalt i låghaltig malm med cirka 5 %. Därför används den endast i kombination med andra typer av berikning.
- Gravity rengöring.
Det utförs med hjälp av speciella typer av suspensioner, vars densitet överstiger densiteten av gråberg, men är sämre än järnets densitet. Under inflytande gravitationskrafter biprodukter stiger till toppen och järn faller till botten av suspensionen.
- Magnetisk separation.
Den vanligaste förädlingsmetoden, som bygger på olika nivåer av uppfattning av malmkomponenter av påverkan av magnetiska krafter. Sådan separation kan utföras med torrt berg, vått berg eller i en alternativ kombination av dess två tillstånd.
För att bearbeta torra och våta blandningar används speciella trummor med elektromagneter.
- Flotation.
För denna metod doppas krossad malm i form av damm i vatten med tillsats av ett speciellt ämne (flotationsreagens) och luft. Under påverkan av reagenset förenas järnet med luftbubblorna och stiger till vattenytan, medan gråberget sjunker till botten. Komponenter som innehåller järn samlas upp från ytan i form av skum.
Mål. Introducera järnets position periodiska systemet kemiska element i D.I. Mendeleev, atomstruktur, naturliga avlagringar, föreningar, moderna produktionsmetoder, egenskaper och användningsområden för järn. Att främja utvecklingen hos skolbarn av färdigheter i kollektivt arbete och kamratligt ömsesidigt bistånd.
Utrustning och reagens. Provrör, tabeller över masugnsproduktion; lösningar av HCl och H 2 SO 4, pulver av Fe(OH) 2 och Fe(OH) 3, järnspån, lösningar av gult blodsalt K 4 och rött blodsalt K 3.
Lektionstyp. Inslag av föreläsning, berättelse, samtal.
UNDER KLASSERNA
Lärare. Idag kommer vi att fortsätta vårt samtal om metaller, du kommer att lära dig om järnets position i det periodiska systemet för kemiska grundämnen, strukturen på dess atom, metallens kemiska egenskaper, dess föreningar, produktion och användning, järnets roll i utvecklingen av det mänskliga samhället. Vilken roll har järn i det mänskliga samhället?
Studerande. Järn spelade en stor roll i utvecklingen av det mänskliga samhället och har inte förlorat sin betydelse idag. Av alla metaller är det den mest använda i modern industri.
Den primitiva människan började använda järnverktyg flera årtusenden f.Kr. Under dessa år var den enda källan till denna metall meteoriter som föll till marken, som innehåller ganska rent järn. I mitten av det 2:a årtusendet f.Kr
n. e. I Egypten bemästrade man järnmetallurgi - utvinning av järnmalm. Denna händelse markerade början av järnåldern i mänsklighetens historia, som ersatte sten- och bronsåldern. På Rysslands territorium går början av järnåldern tillbaka till skiftet av det 2:a–1:a årtusendet f.Kr. e.
Lärare. Hur är fördelningen av järn i naturen?
Studerande. Järn är ett av de vanligaste grundämnena i naturen. I jordskorpan är dess massandel 5,1%, enligt denna indikator är den näst efter syre, kisel och aluminium. Mycket järn finns också i himlakroppar, vilket bestäms genom spektralanalys. I prover av månjord som levererades av den sovjetiska automatiska stationen "Luna" hittades järn i ooxiderat tillstånd..
Lärare. I vilken form förekommer järn i naturen?
Studerande. Järn är en komponent i de flesta stenar. För att få fram järn används järnmalmer med en järnhalt på 30–70 % eller mer.(Använder sig av fysiskt kort Ryssland, studenten visar och namnger avlagringar av järnföreningar.)
De viktigaste järnmalmerna är:
– hematit
Fe 2 O 3 – innehåller upp till 65% järn, sådana järnavlagringar finns i Krivoy Rog-regionen;
– limonit
Fe2O3 n H2O – innehåller upp till 60% järn, limonitavlagringar finns på Krim, till exempel Kerch-fyndigheten;
– pyrit
FeS 2 – innehåller cirka 47% järn, pyritavlagringar finns i Ural.
Lärare. Hur får man järn i industrin?
Studerande. För närvarande är den huvudsakliga industriella metoden för bearbetning av järnmalm produktion av gjutjärn genom masugnsprocessen. Gjutjärnär en järnlegering som innehåller
2,2–4 % kol, samt kisel, mangan, fosfor, svavel. Därefter omvandlas det mesta av gjutjärnet till stål. Stål skiljer sig från gjutjärn främst genom sin lägre kolhalt (upp till 2%), fosfor och svavel.
Lärare. Mycket uppmärksamhet ägnas åt utvecklingen av metoder för direkt produktion av järn från malmer utan masugnsprocessen. Vad är fördelen med att få järn direkt? Huvudsaken är att reduktionen av järnoxider kan utföras utan deltagande av metallurgisk koks. Det ersätts av billigare och vanligare bränslen - brunkol, naturgas. Vid direktframställning av järn kan även låghaltiga järnmalmer och slagg från andra industrier som innehåller järn användas.
Direkt reduktion av järn utförs i lätt lutande roterugnar, liknande de ugnar som används för att tillverka cement. Malm och kol laddas kontinuerligt in i ugnen, som gradvis rör sig till utloppet, uppvärmd luft strömmar i motström, vilket skapar en temperatur under smältpunkten för järn.
För att erhålla tekniskt rent järn genom direkt reduktion utsätts malmen för anrikning. Samtidigt är det möjligt att öka massfraktionen av järn, separera gråberg (järnbitar separeras lätt från slaggen) och minska halten av skadliga föroreningar (svavel och fosfor). Under förädlingsprocessen krossas malmen i krossverk och matas in i en magnetisk separator. Den senare är en trumma med elektromagneter i vilken krossad malm matas in med hjälp av en transportör. Gråberget passerar fritt genom magnetfältet och faller. Malmkornen som innehåller magnetiska järnmineraler magnetiseras och separeras från trumman senare än gänget. Så magnetiskt separation kan göras flera gånger.
Malmen anrikas sedan med metoden flotation. För att göra detta placeras malmen i en behållare med vatten, där flytande ytaktiva ämnen löses, som selektivt absorberas på ytan av det användbara mineralet. Som ett resultat av absorptionen av flotationsreagenset vätas mineralpartiklarna inte av vatten och sjunker inte ner i det. Luft passerar genom lösningen, vars bubblor fäster vid mineralbitarna och lyfter dem till ytan. Partiklar av gråberg vätas väl av vatten och lägger sig i botten av behållaren. Den anrikade malmen samlas upp från lösningens yta tillsammans med skummet. Som ett resultat kan järnhalten i malmen ökas till 70–72 %.
Låt oss överväga ett diagram över en av metoderna för att direkt få järn. Processen utförs i en vertikal ugn, i vilken anrikad malm matas uppifrån och gas, som fungerar som reduktionsmedel, underifrån. Denna gas produceras genom förbränning av naturgas i frånvaro av syre. Reducerande gas innehåller 30% CO , 55%
H 2 ,
13%
H2O och 2 % CO 2 . Därför är reduktionsmedlen kol(II)monoxid CO och väte:
Fe 2 O 3 + 3CO = 2Fe + 3CO 2,
Fe2O3 + 3H2 = 2Fe + 3H2O.
Reduktionen utförs vid en temperatur på 850–900 °C, vilket är lägre än smältpunkten för järn (1539 °C).
Många moderna teknikgrenar kräver väldigt mycket järn hög grad renlighet. Därefter rengörs det tekniska strykjärnet karbonyl metod. Karbonyler är föreningar av metaller med kolmonoxid (II) CO. Järn reagerar med CO vid förhöjt tryck och temperatur på 100–200 °C och bildar järnpentakarbonyl:

Järnpentakarbonyl är en vätska som lätt kan separeras från föroreningar genom destillation. Vid en temperatur på cirka 250 °C sönderdelas karbonyl lätt och bildar järnpulver:
Fe(CO)5 = Fe + 5CO.
Om det resulterande pulvret sintras i vakuum blir resultatet en metall som innehåller 99,98–99,999 % järn. Varför behöver du skaffa metall av sådan renhet?
Studerande. Järn av hög renhetsgrad behövs främst för att studera dess egenskaper, d.v.s. för vetenskapliga ändamål. Om vi inte hade kunnat få tag i rent järn hade vi inte vetat att det var en mjuk, lättbearbetbar metall. Kemiskt rent järn är mycket mer inert än industrijärn. En viktig industri för användningen av rent järn är tillverkningen av speciella ferrolegeringar, vars egenskaper försämras av närvaron av föroreningar.
Lärare. Vilka är de kemiska egenskaperna hos järn?
Studerande. Järns kemiska egenskaper bestäms av strukturen hos atomernas elektroniska skal. Järn är ett element i den sekundära undergruppen VIII i grupp 4 lång period. Järn tillhör d-elementen, den elektroniska formeln för atomen har ändelsen ...3d 6 4s 2. Järn i föreningar uppvisar oxidationstillstånd +2 och +3. Det maximala oxidationstillståndet för järn är +6. Det visar sig i ferrater - salter av icke-existerande järnsyra. Till exempel, Na2FeO4 – natriumferrat.
Lärare. Hur reagerar järn med syre?
Studerande. I den elektrokemiska serien av spänningar är järn till vänster om väte, dvs det har en mer negativ standardelektrodpotential. Därför löser sig järn lätt i saltsyra och utspädda svavelsyror med frisättning av väte:
Fe + 2HCl = FeCl2 + H2,
Fe + H2SO4 (utspädd) = FeSO4 + H2.
Järn reducerar mer koncentrerad svavelsyra (40–60%) till
svavel(IV)oxid:
Fe + 2H2SO4 = FeSO4 + SO2 + 2H2O.
I svavelsyra med ännu högre koncentration (från 80 till 100%) järn passiverat– är täckt med en tunn och hållbar oxidfilm, som skyddar metallen från upplösning. Samma passiveringsfenomen observeras i högkoncentrerad salpetersyra, därför kan koncentrerad svavelsyra och salpetersyra transporteras i järnbehållare.
Med utspädd salpetersyra järn kan reagera för att bilda ett järn(II)salt, och med en mer koncentrerad syralösning - ett järn(III)salt och olika syreduktionsprodukter, till exempel:
4Fe + 10HNO3 = 4Fe(NO3)2 + NH4NO3 + 3H2O,
3Fe + 8HNO3 = 3Fe(NO3)2 + 2NO + 4H2O,
Fe + 6HNO3 = Fe(NO3)3 + 3NO2 + 3H2O.
Lärare. Kom ihåg vad som kallas korrosion. Vilka är dess konsekvenser?
Studerande. Korrosion är förstörelse av metall under påverkan av miljön. Bildandet av rost kan representeras enligt följande:
4Fe + 3O2 + 6H2O = 4Fe(OH)3,

Rost lossnar från metallytan, har många porer och skyddar därför inte metallen från ytterligare korrosion. På grund av korrosion förstörs en enorm mängd järn och dess legeringar. På 1800-talet, när det inte fanns några tillförlitliga metoder för att bekämpa korrosion, försvann hälften av den smälta metallen från den. Under moderna förhållanden dör 1/6 av det producerade gjutjärnet från korrosion. Därför är kampen mot korrosion en av mänsklighetens viktigaste uppgifter..
Lärare. Är järnföreningar amfotära?
(Frågan som ställs kan besvaras av läraren själv eller av en tidigare förberedd elev som är intresserad av kemi.)
Järn(III)hydroxid är amfoter, dvs den uppvisar egenskaperna hos en bas i reaktion med syror:
Fe(OH)3 + 3HCl = FeCl3 + 3H2O,
och sura egenskaper i reaktioner med koncentrerade alkalilösningar:
Järn(III)oxid har också en amfotär karaktär, som reagerar med både syror och basiska oxider:
Fe2O3 + 6HCl = 2FeCl3 + 3H2O,
![]()
Läraren uppmärksammar eleverna på det faktum att det finns karakteristiska reaktioner på föreningar av tvåvärt och trevärt järn, vilket åtföljer hans berättelse med experiment.
Lärare. För att detektera järn(III)-joner är det lämpligt att använda en järnkomplexförening som kallas gult blodsalt eller kaliumhexacyanoferrat(II). K4. När joner interagerar(Fe(CN) 6) 4– med joner Fe 3+ en mörkblå fällning bildas - preussisk blå:

En annan järnförening är rött blodsalt eller kaliumhexacyanoferrat(III) K 3 är ett reagens för joner Fe2+.
När joner interagerar(Fe(CN) 6) 3– med joner Fe 2+ en mörkblå fällning bildas också - Turnboole blue:

Lista de huvudsakliga användningsområdena för järn. Vilken är den naturliga betydelsen av järn?
(Elever svarar på frågorna, läraren förklarar sina svar.)
Första studenten. Ferrater av olika metaller används i moderna industrier av radioelektronik och automation..
Andra elev. Järn bildar ovanliga föreningar med väte, kväve och kol. Atomerna i dessa icke-metaller är mindre i storlek än järnatomer och introduceras lätt mellan noderna i metallkristallgittret och bildar mellanliggande fasta lösningar.

Mellanliggande fasta lösningar liknar metall, men deras egenskaper skiljer sig mycket från järns. För det mesta Dessa är mycket hårda och spröda ämnen. Järn bildar hydrider med väte FeH Och FeH2, med kväve - nitrider Fe4N Och Fe2N , med kol – karbid Fe 3 C – cementit i gjutjärn och stål.
Tredje elev. Järn är en metall vars användning i industrin och vardagen inte har några gränser. Stål används ofta i modern teknik. Järnoxider och salter används vid tillverkning av färger, magnetiska material, katalysatorer, mediciner och gödningsmedel.
Fjärde elev. Utan järn kan människokroppen inte fungera, den innehåller cirka 3–4 g järn, varav 2 g finns i blodet.Järn ingår i hemoglobinet. Otillräckligt järninnehåll i människokroppen leder till huvudvärk, trötthet och andra sjukdomar. Järn är också nödvändigt för växternas tillväxt. I allmänhet är järn för närvarande den viktigaste metallen i betydelse.
För att konsolidera det studerade materialet erbjuds studenterna följande: frågor.
1. Vilken position har järn i det periodiska systemet för kemiska grundämnen?
2. Vilka oxidationstillstånd uppvisar järn i föreningar?
3. Vilka järnföreningar har amfotära egenskaper?
4. Hur reagerar järn med salpeter- och svavelsyror i olika koncentrationer?
5. Hur skiljer man på tvåvärda och trevärda järnföreningar?
6. Vilken är användningen och betydelsen av järnföreningar på det nuvarande stadiet av mänsklig utveckling?Om tiden tillåter kan du konsolidera det aktuella materialet för tillverkning av järn med hjälp av följande frågor.
1. Vilken är fördelen med den direkta metoden för att få fram järn?
2. Vad används malmförädling till?
3. Hur anrikas malm genom flotation?
4. Vad är huvudsyftet med att rena industrijärn med karbonylmetoden?
LITTERATUR
Läsebok om oorganisk kemi. Comp. V.A.Kritsman, M.: Utbildning, 1984;
Feldman F.G., Rudzitis G.E. Kemi. Lärobok för 9:e klass av allmänna läroanstalter. M.: Utbildning, 1999;
Khomchenko G.P. Kemi för dem som går in på universitet. M.: Högre skola, 1993.
- I kontakt med 0
- Google+ 0
- OK 0
- Facebook 0