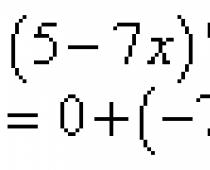Vattenegenskaper och dess roll i cellen:
I första hand bland cellens substanser är vatten. Den utgör cirka 80 % av cellmassan. Vatten är dubbelt viktigt för levande organismer, eftersom det är nödvändigt inte bara som en del av celler, utan för många och som livsmiljö.
1. Vatten avgör fysikaliska egenskaper celler - dess volym, elasticitet.
2. Många kemiska processer sker endast i vattenlösning.
3. Vatten är ett bra lösningsmedel: många ämnen kommer in i cellen från den yttre miljön i en vattenlösning och i en vattenlösning avlägsnas avfallsprodukter från cellen.
4. Vatten har hög värmekapacitet och värmeledningsförmåga.
5. Vatten har en unik egenskap: när det kyls från +4 till 0 grader expanderar det. Därför visar sig isen vara lättare än flytande vatten och ligger kvar på ytan. Detta är mycket viktigt för organismer som lever i vattenmiljön.
6. Vatten kan vara ett bra smörjmedel.
Vattnets biologiska roll bestäms av den lilla storleken på dess molekyler, deras polaritet och förmågan att kombinera med varandra genom vätebindningar.
Biologiska funktioner av vatten:
transport. Vatten säkerställer förflyttning av ämnen i cellen och kroppen, absorptionen av ämnen och utsöndringen av metaboliska produkter. I naturen transporterar vatten avfallsprodukter till jordar och vattendrag.
metabolisk. Vatten är mediet för all bio kemiska reaktioner, elektrondonator för fotosyntes; det är nödvändigt för hydrolysen av makromolekyler till deras monomerer.
vatten deltar i bildningen av smörjande vätskor och slem, sekret och safter i kroppen.
Med mycket få undantag (ben och tandemalj) är vatten den dominerande komponenten i cellen. Vatten är nödvändigt för metabolismen (utbytet) av cellen, eftersom fysiologiska processer uteslutande sker i vattenmiljön. Vattenmolekyler är involverade i många enzymatiska reaktioner i cellen. Till exempel sker nedbrytningen av proteiner, kolhydrater och andra ämnen som ett resultat av deras interaktion med vatten som katalyseras av enzymer. Dessa reaktioner kallas hydrolysreaktioner.
Vatten fungerar som en källa till vätejoner i fotosyntesen. Vattnet i cellen finns i två former: fritt och bundet. Fritt vatten utgör 95 % av allt vatten i cellen och används huvudsakligen som lösningsmedel och som dispersionsmedium för protoplasmans kolloidala system. Bundet vatten, som bara står för 4% av allt cellvatten, är löst vätebundet till proteiner.
På grund av den asymmetriska fördelningen av laddningar fungerar vattenmolekylen som en dipol och kan därför bindas både positivt och negativt laddade grupper av proteinet. En vattenmolekyls dipolegenskap förklarar dess förmåga att orientera sig i ett elektriskt fält, att fästa vid olika molekyler och delar av molekyler som bär en laddning. Som ett resultat bildas hydrater
På grund av sin höga värmekapacitet absorberar vatten värme och förhindrar därmed plötsliga temperatursvängningar i buren. Vattenhalten i kroppen beror på dess ålder och metaboliska aktivitet. Den är högst i embryot (90 %) och minskar gradvis med åldern. Vattenhalten i olika vävnader varierar beroende på deras metaboliska aktivitet. Till exempel, i hjärnans grå substans är vatten upp till 80% och i benen upp till 20%. Vatten är huvudmedlet för rörelse av ämnen i kroppen (flödet av blod, lymfa, stigande och nedåtgående strömmar av lösningar genom växtkärlen) och i cellen. Vatten fungerar som ett "smörjmedel" som är väsentligt varhelst det finns gnidningsytor (till exempel i lederna). Vatten har en maximal densitet vid 4 ° C. Därför är is, som har en lägre densitet, lättare än vatten och flyter på dess yta, vilket skyddar reservoaren från att frysa. Denna egenskap hos vatten räddar livet på många vattenlevande organismer.
1. Vilken struktur har vatten?
Svar. Vattenmolekylen har en vinkelstruktur: kärnorna som ingår i dess sammansättning bildar en likbent triangel, vid basen av vilken det finns två väten, och i spetsen finns en syreatom. Internuclear O-N avståndär nära 0,1 nm, är avståndet mellan kärnorna av väteatomer 0,15 nm. Av de sex elektroner som utgör den yttre elektroniskt lager syreatom i en vattenmolekyl bildar två elektronpar kovalenta kommunikation O-N, och de andra fyra elektronerna representerar två ensamma elektronpar.
En vattenmolekyl är en liten dipol som innehåller positiva och negativa laddningar vid polerna. Det finns en brist på elektrontäthet nära vätekärnorna, och ett överskott av elektrondensitet observeras på motsatt sida av molekylen, nära syrekärnan. Det är denna struktur som bestämmer vattenmolekylens polaritet.
2. Hur mycket vatten (i%) finns i olika celler?
Mängden vatten är inte densamma i olika vävnader och organ. Så hos människor är dess innehåll i hjärnans grå substans 85% och i benvävnad - 22%. Den högsta vattenhalten i kroppen observeras under embryonalperioden (95%) och minskar gradvis med åldern.
Vattenhalten i olika växtorgan varierar inom ganska vida gränser. Det förändras beroende på miljöförhållanden, ålder och växtarter. Så vattenhalten i salladsblad är 93-95%, majs - 75-77%. Mängden vatten är inte densamma i olika växtorgan: i solrosbladen innehåller vatten 80-83%, i stjälkarna - 87-89%, i rötterna - 73-75%. Vattenhalten, lika med 6-11%, är typiskt främst för lufttorka frön, där vitala processer hämmas. Vatten finns i levande celler, i döda xylemelement och i intercellulära utrymmen. I de intercellulära utrymmena är vatten i ett ångformigt tillstånd. Växtens huvudsakliga förångningsorgan är bladen. I detta avseende är det naturligt att den största mängden vatten fyller bladens intercellulära utrymmen. I flytande tillstånd finns vatten i olika delar av cellen: cellmembranet, vakuolerna, cytoplasman. Vakuoler är den rikaste delen av cellen med vatten, där dess innehåll når 98%. Med den högsta vattenhalten är vattenhalten i cytoplasman 95%. Den lägsta vattenhalten är karakteristisk för cellmembranen. Det är svårt att kvantifiera vattenhalten i cellmembranen; uppenbarligen varierar det från 30 till 50%. Vattenformerna i olika delar av växtcellen är också olika.
3. Vilken roll har vattnet i levande organismer?
Svar. Vatten är den dominerande komponenten i alla levande organismer. Den har unika egenskaper på grund av dess strukturella egenskaper: vattenmolekyler är dipolformade och vätebindningar bildas mellan dem. Den genomsnittliga vattenhalten i cellerna hos de flesta levande organismer är cirka 70 %. Vatten i cellen finns i två former: fritt (95 % av allt cellvatten) och bundet (4-5 % bundet till proteiner).
Vattens funktioner:
1. Vatten som lösningsmedel. Många kemiska reaktioner i cellen är joniska, så de sker bara i vattenmiljön. Ämnen som löser sig i vatten kallas hydrofila (alkoholer, sockerarter, aldehyder, aminosyror), olösliga - hydrofoba (fettsyror, cellulosa).
2. Vatten som reagens. Vatten är involverat i många kemiska reaktioner: polymerisationsreaktioner, hydrolys, i processen för fotosyntes.
3. Transportfunktion. Förflyttning av ämnen lösta i den genom kroppen tillsammans med vatten till dess olika delar och avlägsnande av onödiga produkter från kroppen.
4. Vatten som termostabilisator och termostat. Denna funktion beror på sådana egenskaper hos vatten som hög värmekapacitet - mjukar upp effekten på kroppen av betydande temperaturförändringar i miljön; hög värmeledningsförmåga - gör att kroppen kan bibehålla samma temperatur genom hela sin volym; hög förångningsvärme - används för att kyla kroppen under svett hos däggdjur och transpiration i växter.
5. Strukturell funktion. Cellernas cytoplasma innehåller från 60 till 95 % vatten, och det är detta som ger cellerna deras normal form... Hos växter upprätthåller vattnet turgor (elasticiteten hos det endoplasmatiska membranet), hos vissa djur fungerar det som ett hydrostatiskt skelett (maneter)
Frågor efter 7 §
1. Vad är särdraget med vattenmolekylens struktur?
Svar. Vattens unika egenskaper bestäms av strukturen på dess molekyl. En vattenmolekyl består av en O-atom bunden till två H-atomer genom polära kovalenta bindningar. Det karakteristiska arrangemanget av elektroner i en vattenmolekyl ger den elektrisk asymmetri. Den mer elektronegativa syreatomen attraherar väteatomernas elektroner starkare, vilket resulterar i att de gemensamma elektronparen förskjuts i vattenmolekylen i dess riktning. Därför, även om vattenmolekylen som helhet inte är laddad, har var och en av de två väteatomerna en delvis positiv laddning (betecknad med 8+), och syreatomen har en delvis negativ laddning (8-). Vattenmolekylen är polariserad och är en dipol (har två poler).
Den delvis negativa syreatomen i en vattenmolekyl attraheras av de delvis positiva väteatomerna i andra molekyler. Således tenderar varje vattenmolekyl att vätebindas med fyra närliggande vattenmolekyler.
2. Vilken betydelse har vatten som lösningsmedel?
Svar. På grund av molekylernas polaritet och förmågan att bilda vätebindningar löser vatten lätt jonföreningar (salter, syror, baser). Vissa nonjoniska men polära föreningar löser sig också bra i vatten, dvs i vars molekyl laddade (polära) grupper finns närvarande, till exempel sockerarter, enkla alkoholer, aminosyror. Ämnen som är lättlösliga i vatten kallas hydrofila (av grekiskan hygros - fuktig och philia - vänskap, böjelse). När ett ämne går i lösning kan dess molekyler eller joner röra sig mer fritt och därför ökar ämnets reaktivitet. Detta förklarar varför vatten är det huvudsakliga mediet där de flesta kemiska reaktioner äger rum, och alla hydrolysreaktioner och många redoxreaktioner äger rum med direkt deltagande av vatten.
Ämnen som är dåligt eller helt olösliga i vatten kallas hydrofoba (av grekiskan phobos - rädsla). Dessa inkluderar fetter, nukleinsyror, vissa proteiner och polysackarider. Sådana ämnen kan bilda gränssnitt med vatten, på vilka många kemiska reaktioner äger rum. Därför är det faktum att vatten inte löser opolära ämnen också mycket viktigt för levande organismer. Bland de fysiologiskt viktiga egenskaperna hos vatten är dess förmåga att lösa upp gaser (О2, СО2, etc.).
3. Vilken är vattnets värmeledningsförmåga och värmekapacitet?
Svar. Vatten har en hög värmekapacitet, det vill säga förmågan att absorbera värmeenergi med en minimal ökning av sin egen temperatur. Vattnets höga värmekapacitet skyddar kroppsvävnader från snabb och kraftig temperaturökning. Många organismer kyls ner genom att vatten avdunstar (transpiration i växter, svett hos djur).
4. Varför tror de att vatten är idealisk vätska för en cell?
Svar. Den höga vattenhalten i cellen är den viktigaste förutsättningen för dess aktivitet. Med förlusten av det mesta av vattnet dör många organismer, och ett antal encelliga och till och med flercelliga organismer förlorar tillfälligt alla tecken på liv. Detta tillstånd kallas avstängd animering. Efter hydrering vaknar cellerna och blir aktiva igen.
Vattenmolekylen är elektriskt neutral. Men den elektriska laddningen inuti molekylen är ojämnt fördelad: i området för väteatomer (mer exakt, protoner), Positiv laddning, i området där syre finns är den negativa laddningstätheten högre. Därför är en vattenpartikel en dipol. En vattenmolekyls dipolegenskap förklarar dess förmåga att orientera sig i ett elektriskt fält, att fästa vid olika molekyler och delar av molekyler som bär en laddning. Som ett resultat bildas hydrater. Vattens förmåga att bilda hydrater beror på dess universella upplösningsegenskaper. Om attraktionsenergin för vattenmolekyler till molekyler av något ämne är större än attraktionsenergin mellan vattenmolekyler, då löses ämnet. Beroende på detta finns det hydrofila (grekiska hydros - vatten och phileo - jag älskar) ämnen som är lättlösliga i vatten (till exempel salter, alkalier, syror, etc.), och hydrofoba (grekiska hydros - vatten och fobos - rädsla ) ämnen, knappt eller inte alls lösliga i vatten (fetter, fettliknande ämnen, gummi, etc.). I cellmembranens sammansättning ingår fettliknande ämnen som begränsar övergången från den yttre miljön till cellerna och vice versa, samt från en del av cellen till en annan.
De flesta av de reaktioner som sker i cellen kan endast ske i en vattenlösning. Vatten är en direkt deltagare i många reaktioner. Till exempel sker nedbrytningen av proteiner, kolhydrater och andra ämnen som ett resultat av deras interaktion med vatten som katalyseras av enzymer. Sådana reaktioner kallas hydrolysreaktioner (grekiska hydros - vatten och lysis - splittring).
Vatten har en hög värmekapacitet och samtidigt en relativt hög värmeledningsförmåga för vätskor. Dessa egenskaper gör vatten till en idealisk vätska för att upprätthålla termisk jämvikt mellan cellen och kroppen.
Vatten är det huvudsakliga mediet för cellens biokemiska reaktioner. Det är en källa till syre som frigörs under fotosyntesen och väte, som används för att återställa assimileringsprodukter. koldioxid... Och slutligen är vatten det huvudsakliga medlet för rörelse av ämnen i kroppen (flödet av blod och lymfa, stigande och nedåtgående strömmar av lösningar genom växtkärlen) och i cellen.
5. Vilken roll har vattnet i cellen
Säkerställer cellelasticitet. Konsekvenserna av cellens förlust av vatten är vissnande av löv, torkning av frukter;
Acceleration av kemiska reaktioner på grund av upplösning av ämnen i vatten;
Säkerställa förflyttning av ämnen: införandet av de flesta ämnen i cellen och deras avlägsnande från cellen i form av lösningar;
Säkerställa upplösningen av många kemikalier (ett antal salter, sockerarter);
Deltagande i ett antal kemiska reaktioner;
Deltagande i processen för värmereglering på grund av förmågan att långsam uppvärmning och långsam nedkylning.
6. Vilka är de strukturella och fysiska Kemiska egenskaper vatten bestämma dess biologiska roll i cellen?
Svar. Vattens strukturella fysikalisk-kemiska egenskaper bestämmer dess biologiska funktioner.
Vatten är ett bra lösningsmedel. På grund av molekylernas polaritet och förmågan att bilda vätebindningar löser vatten lätt jonföreningar (salter, syror, baser).
Vatten har en hög värmekapacitet, det vill säga förmågan att absorbera värmeenergi med en minimal ökning av sin egen temperatur. Vattnets höga värmekapacitet skyddar kroppsvävnader från snabb och kraftig temperaturökning. Många organismer kyls ner genom att vatten avdunstar (transpiration i växter, svett hos djur).
Vatten har också en hög värmeledningsförmåga, vilket säkerställer en jämn fördelning av värme i hela kroppen. Följaktligen gör den höga specifika värmen och den höga värmeledningsförmågan vatten till en idealisk vätska för att upprätthålla termisk jämvikt mellan cellen och kroppen.
Vatten komprimerar praktiskt taget inte, skapar turgortryck, bestämmer volymen och elasticiteten hos celler och vävnader. Så det är det hydrostatiska skelettet som behåller sin form hos rundmaskar, maneter och andra organismer.
Vatten kännetecknas av värdet av den ytspänningskraft som är optimal för biologiska system, som uppstår på grund av bildandet av vätebindningar mellan vattenmolekyler och molekyler av andra ämnen. På grund av kraften från ytspänning uppstår kapillärt blodflöde, stigande och fallande strömmar av lösningar i växter.
I vissa biokemiska processer fungerar vatten som ett substrat.
Vatten är den mest utbredda kemiska föreningen på jorden, dess massa är den största i en levande organism. Det uppskattas att vatten är 85 % av total massa sredneostatis -tichesky cell. I mänskliga celler är vatten i genomsnitt cirka 64 %. Vattenhalten i olika celler kan dock variera avsevärt: från 10 % i tandemaljens celler till 90 % i däggdjursembryots celler. Dessutom innehåller unga celler mer vatten än gamla. Så i en babys celler är vatten 86%, i cellerna hos en gammal person, bara 50%.
Hos hanar är vattenhalten i burarna i genomsnitt 63 %, hos honor något mindre än 52 %. Vad orsakade detta? Det visar sig att allt är enkelt. I den kvinnliga kroppen finns det mycket fettvävnad, i cellerna där det finns lite vatten. Därför är vattenhalten i kvinnokroppen cirka 6-10% lägre än hos hanen.
Vattens unika egenskaper beror på strukturen hos dess molekyl. Från kemins gång vet du att den olika elektronegativiteten hos väte- och syreatomer är orsaken till uppkomsten av kovalenta polär anslutning i en vattenmolekyl. Vattenmolekylen har formen av en triangel (87), i vilken elektriska laddningar arrangerad asymmetriskt, och är en dipol (kom ihåg definitionen av denna term).
På grund av den elektrostatiska attraktionen av väteatomen i en vattenmolekyl till syreatomen i en annan molekyl, uppstår vätebindningar mellan vattenmolekylerna.
Egenskaperna hos vattnets struktur och fysikalisk-kemiska egenskaper (vattens förmåga att vara ett universellt lösningsmedel, variabel densitet, hög värmekapacitet, stor ytspänning, fluiditet, kapilläritet, etc.), som bestämmer dess biologiska betydelse.
Vilka funktioner har vatten i kroppen Vatten är ett lösningsmedel. Vattenmolekylens polära struktur förklarar dess egenskaper som lösningsmedel. Vattenmolekyler interagerar med kemiska ämnen, vars element har elektrostatiska bindningar, och bryter ner dem till anjoner och katjoner, vilket leder till kemiska reaktioner. Som ni vet sker många kemiska reaktioner endast i vattenlösning. Samtidigt förblir vattnet i sig inert, därför kan det användas i kroppen upprepade gånger. Vatten fungerar som ett medium för att transportera olika ämnen in i kroppen. Dessutom utsöndras slutprodukterna av ämnesomsättningen från kroppen huvudsakligen i upplöst form.
Det finns två huvudtyper av lösningar i levande varelser. (Kom ihåg klassificeringen av lösningar.)
Den så kallade sanna lösningen, när lösningsmedelsmolekylerna sammanfaller i storlek med det lösliga ämnets molekyler, löses de upp. Som ett resultat uppstår dissociation och joner bildas. I det här fallet är lösningen homogen och, i vetenskapliga termer, består den av en - den flytande fasen. Typiska exempelär lösningar av mineralsalter, syror eller alkalier. Eftersom det finns laddade partiklar i sådana lösningar kan de leda elektricitet och är elektrolyter, som alla lösningar som finns i kroppen, inklusive blod från ryggradsdjur, som innehåller många mineralsalter.
Kolloidal lösning är fallet när lösningsmedelsmolekylerna är mycket mindre i storlek än de lösta molekylerna. I sådana lösningar rör sig partiklar av ett ämne, som kallas kolloidalt, fritt i vattenpelaren, eftersom kraften i deras attraktion inte överstiger styrkan hos deras bindningar med lösningsmedelsmolekyler. En sådan lösning anses heterogen, det vill säga bestående av två faser - flytande och fast. Alla biologiska vätskor är blandningar som innehåller sanna och kolloidala lösningar, eftersom de innehåller både mineralsalter och enorma molekyler (till exempel proteiner), som har egenskaperna hos kolloidala partiklar. Därför innehåller cytoplasman av någon cell, blod eller lymf från djur, mjölk från däggdjur samtidigt joner och kolloidala partiklar.
Som du säkert kommer ihåg lyder biologiska system alla fysiks och kemilagar, därför observeras fysiska fenomen i biologiska lösningar som spelar en betydande roll i organismers liv.
Vattenegenskaper
Diffusion (från lat. Diffusion - spridning, spridning, dispergering) i biologiska lösningar visar sig som en tendens att utjämna koncentrationen av strukturella partiklar av lösta ämnen (joner och kolloidala partiklar), vilket i slutändan leder till en jämn fördelning av ämnet i lösning. Det är tack vare diffusion som många encelliga varelser matas, syre och näringsämnen transporteras genom djurkroppen i avsaknad av cirkulations- och andningssystemet i dem (kom ihåg vilken typ av djur de är). Dessutom sker transporten av många ämnen till cellerna just på grund av diffusion.
En till fysiskt fenomen- osmos (från grekiskan. Osmos - tryck, tryck) - lösningsmedlets rörelse genom ett semipermeabelt membran. Osmos gör att vatten flyttar ut ur en lösning med låg koncentration av lösta ämnen och hög halt av H20 i en lösning med hög koncentration av lösta ämnen och låg vattenhalt. V biologiska system det är inget annat än transport av vatten på cellens nivå. Det är därför osmos spelar en betydande roll hos många biologiska processer... Osmosens kraft säkerställer rörelsen av vatten i växt- och djurorganismer, på grund av vilket deras celler får näring och bibehåller en konstant form. Det bör noteras att ju större skillnaden är i koncentrationen av ett ämne, desto större är det osmotiska trycket. Därför, om cellerna placeras i en hypoton lösning, sväller de och brister på grund av det plötsliga inflödet av vatten.
Den vitala aktiviteten hos celler, vävnader och växtorgan beror på närvaron av vatten. Vatten är ett konstitutionellt ämne. Bestämning av strukturen av cytoplasman hos celler och dess organeller, på grund av molekylernas polaritet, är det ett lösningsmedel för organiska och oorganiska föreningar som är involverade i metabolism och fungerar som en bakgrundsmiljö där alla biokemiska processer äger rum. Vattnet tränger lätt igenom cellernas membran och membran och cirkulerar fritt genom växten, vilket säkerställer överföring av ämnen och bidrar därmed till enheten i kroppens metaboliska processer. På grund av dess höga transparens stör vatten inte absorptionen av solenergi av klorofyll.
Vattentillstånd i växtceller
Vattnet i cellen presenteras i flera former, som är fundamentalt olika. De viktigaste är konstitutionellt, solvat-, kapillär- och reservvatten.
Några av vattenmolekylerna som kommer in i cellen bildar vätebindningar med ett antal molekylradikaler organiskt material... Följande radikaler bildar särskilt lätt vätebindningar:
Denna form av vatten brukar kallas konstitutionell . Den finns i en bur med en styrka på upp till 90 tusen fat.
På grund av det faktum att vattenmolekyler är dipoler, bildar de integrerade aggregat med laddade molekyler av organiska ämnen. Sådant vatten, associerat med molekyler av organiska ämnen i cytoplasman av krafterna från elektrisk attraktion, kallas solvat . Beroende på typ av växtcell står solvat vatten för 4 till 50 % av dess totala mängd. Solvatvatten, liksom konstitutionellt vatten, har ingen rörlighet och är inte ett lösningsmedel.
Mycket av cellens vatten är kapillär , eftersom det ligger i hålrummen mellan makromolekyler. Solvat och kapillärvatten hålls kvar av cellen med en kraft som kallas matrispotential. Det är lika med 15-150 bar.
Boka kalla vattnet inuti vakuolerna. Innehållet av vakuoler är en lösning av sockerarter, salter och en rad andra ämnen. Därför hålls reservvattnet kvar av cellen med en kraft som bestäms av storleken på den osmotiska potentialen för det vakuolära innehållet.
Vattenupptag av växtceller
Eftersom det inte finns några aktiva bärare för vattenmolekyler i celler, utförs dess rörelse in i och ut ur celler, såväl som mellan närliggande celler, endast enligt diffusionslagarna. Därför är koncentrationsgradienterna för lösta ämnen huvudmotorerna för vattenmolekyler.
Växtceller, beroende på deras ålder och tillstånd, absorberar vatten genom sekventiell aktivering av tre mekanismer: imbibition, solvatisering och osmos.
Imbibition . När fröna gror börjar de absorbera vatten på grund av uppsugningsmekanismen. I det här fallet fylls de lediga vätebindningarna av organiska ämnen i protoplasten, och vatten strömmar aktivt från miljön in i cellen. Jämfört med andra krafter som verkar i celler är de imbibitionella krafterna kolossala. För vissa vätebindningar når de 90 tusen fat. Dessutom kan frön svälla och gro i relativt torra jordar. Efter att ha fyllt alla lediga vätebindningar, upphör uppsugning och nästa vattenabsorptionsmekanism aktiveras.
Lösning . I solvatiseringsprocessen sker vattenabsorption genom att bygga hydratiseringsskikt runt molekylerna av organiska ämnen i protoplasten. Den totala vattenhalten i buren fortsätter att öka. Solvatiseringens intensitet beror avsevärt på den kemiska sammansättningen av protoplasten. Ju fler hydrofila ämnen i cellen, desto mer fullständigt används solvatiseringskrafterna. Hydrofilicitet minskar i följande ordning: proteiner -> kolhydrater -> fetter. Därför absorberar den största mängden vatten per viktenhet genom solvatisering proteinfrön (ärtor, bönor, bönor), mellanliggande - stärkelsehaltiga frön (vete, råg) och minst - oljefrön (lin, solros).
Lösningskrafterna är underlägsna i kraft än imbibitionens krafter, men de är fortfarande ganska betydande och når 100 bar. I slutet av solvatiseringsprocessen är vattenhalten i cellen så stor att kapillärfuktighet etableras, vakuoler börjar dyka upp. Men från ögonblicket för deras bildande upphör lösningen, och ytterligare absorption av vatten är endast möjlig på grund av den osmotiska mekanismen.
Osmos . Den osmotiska mekanismen för vattenabsorption fungerar bara i celler som har en vakuol. Riktningen för vattenrörelsen i detta fall bestäms av förhållandet mellan de osmotiska potentialerna för lösningarna som ingår i det osmotiska systemet.
Cellsaftens osmotiska potential, betecknad med R, bestäms av formeln:
R = iRcT,
var R - cellsavens osmotisk potential
R - gaskonstant lika med 0,0821;
T - temperatur på Kelvin-skalan;
i- isotonisk koefficient som anger karaktären elektrolytisk dissociation lösta ämnen.
Den isotoniska koefficienten i sig är
och= 1 + α ( n + 1),
där α - graden av elektrolytisk dissociation;
P - antalet joner som molekylen dissocierar i. För icke-elektrolyter P = 1.
Den osmotiska potentialen för en jordlösning betecknas vanligtvis med den grekiska bokstaven π.
Vattenmolekyler rör sig alltid från ett medium med lägre osmotisk potential till ett medium med högre osmotisk potential. Så, om cellen är i en jordlösning (extern) kl P>π, då kommer vatten in i cellerna. Flödet av vatten in i cellen upphör när de osmotiska potentialerna är helt utjämnade (vakuolsaften späds ut vid ingången till absorptionen av vatten) eller när cellmembranet når töjbarhetsgränserna.
Således tar celler emot vatten från omgivningen endast under ett villkor: cellsaftens osmotiska potential måste vara högre än den omgivande lösningens osmotiska potential.
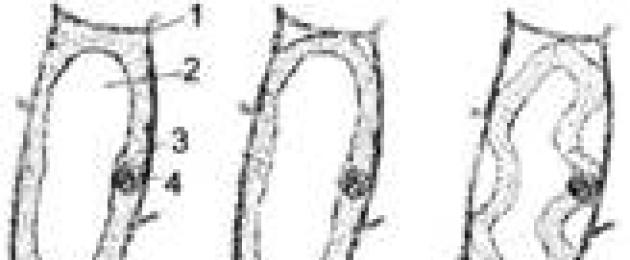
Om R< π, det finns ett utflöde av vatten från cellen till den externa lösningen. Under vätskeförlusten minskar protoplastens volym gradvis, den rör sig bort från membranet och små hålrum uppstår i cellen. Detta tillstånd kallas Plasmolys . Stadierna av plasmolys visas i fig. 3.18.
Om förhållandet mellan osmotiska potentialer motsvarar villkoret P = π sker ingen diffusion av vattenmolekyler alls.
En stor mängd faktamaterial tyder på att den osmotiska potentialen hos växternas cellsav varierar inom ganska vida gränser. I jordbruksväxter i rotceller ligger den vanligtvis i en amplitud på 5-10 bar, i bladceller kan den stiga upp till 40 bar och i fruktceller - upp till 50 bar. I saltmarksväxter når cellsavens osmotiska potential 100 bar.

Ris. 3.18.
A - en cell i ett tillstånd av turgor; B - hörn; B - konkav; G - konvex; D - konvulsiv; E - cap. 1 - skal; 2 - vakuol; 3 - cytoplasma; 4 - kärna; 5 - trådar av Hecht
1.3 Vattenfördelning i buren
Vattenhalten i olika växtorgan varierar inom ganska vida gränser. Det förändras beroende på miljöförhållanden, ålder och växtarter. Så vattenhalten i salladsblad är 93-95%, majs - 75-77%. Mängden vatten är inte densamma i olika växtorgan: i solrosbladen innehåller vatten 80-83%, i stjälkarna - 87-89%, i rötterna - 73-75%. Vattenhalten, lika med 6-11%, är typiskt främst för lufttorka frön, där vitala processer hämmas.
Vatten finns i levande celler, i döda xylemelement och i intercellulära utrymmen. I de intercellulära utrymmena är vatten i ett ångformigt tillstånd. Växtens huvudsakliga förångningsorgan är bladen. I detta avseende är det naturligt att den största mängden vatten fyller bladens intercellulära utrymmen. I flytande tillstånd finns vatten i olika delar av cellen: cellmembran, vakuol, protoplasma. Vakuoler är den rikaste delen av cellen med vatten, där dess innehåll når 98%. Med den högsta vattenhalten är vattenhalten i protoplasman 95 %. Den lägsta vattenhalten är karakteristisk för cellmembranen. Det är svårt att kvantifiera vattenhalten i cellmembranen; uppenbarligen varierar det från 30 till 50%.
Vattenformerna i olika delar av växtcellen är också olika. Vakuolär cellsav domineras av vatten som hålls av föreningar med relativt låg molekylvikt (osmotiskt bundna) och fritt vatten. I skalet på en växtcell är vatten huvudsakligen bundet av högpolymera föreningar (cellulosa, hemicellulosa, pektinämnen), det vill säga kolloidbundet vatten. I själva cytoplasman finns fritt vatten, kolloid och osmotiskt bundet. Vatten som ligger på ett avstånd av upp till 1 nm från ytan av proteinmolekylen är fast bundet och har inte en regelbunden hexagonal struktur (kolloidbundet vatten). Dessutom finns det en viss mängd joner i protoplasman, och därför är en del av vattnet osmotiskt bundet.
Den fysiologiska betydelsen av fritt och bundet vatten är olika. De flesta forskare tror att intensiteten i fysiologiska processer, inklusive tillväxthastigheter, främst beror på innehållet av fritt vatten. Det finns ett direkt samband mellan innehållet av bundet vatten och växternas motståndskraft mot ogynnsamma yttre förhållanden. Dessa fysiologiska korrelationer observeras inte alltid.
Golgiapparat
Golgiapparat
Lysosomer är små vesiklar omgivna av ett enda membran. De knoppar av från Golgi-apparaten och möjligen från det endoplasmatiska retikulumet. Lysosomer innehåller en mängd olika enzymer som bryter ner stora molekyler ...
Skolbarns hälsa: problem och lösningar
När en tonåring ägnar sig åt sport bör överträning inte tillåtas. Trötthet efter intensiv fysisk ansträngning indikeras av letargi, muskelsmärta. Föräldrar bör kontrollera tiden för sport ...
Informationssystem celler
Genetisk information är kodad i DNA. Den genetiska koden upptäcktes av M. Nirenberg och H.G. Koranen, för vilken de tilldelades Nobelpriset 1968. Genetisk kod är ett system för arrangemang av nukleotider i nukleinsyramolekyler ...
Kodning och implementering av biologisk information i en cell, genetisk kod och dess egenskaper
Transmissionsförmedlare genetisk information(nukleotidordning) mRNA (budbärar-RNA) kommer från DNA till protein ...
Meiobentos av makrofytsnår i kustzonen i Novorossiysk-bukten
Det finns många verk som beskriver regelbundenheterna i den rumsliga fördelningen av meiobentosorganismer - under de senaste decennierna har det varit en av de mest populära riktningarna inom forskning ...
År 1890 föreslog Wilhelm Ostwald, som arbetade med semipermeabla konstgjorda filmer, att semipermeabilitet kunde vara orsaken inte bara till osmos, utan också till elektriska fenomen. Osmos uppstår då...
Mikrobiologi av fisk och fiskprodukter
Mikrobiologisk bedömning av vatten ges på basis av bestämning av mikrobiella antalet KMAFAnM; koli - titer; koli - index; förekomsten av patogena mikroorganismer. De två första analyserna utförs ständigt ...
Molekylärgenetisk nivå av levande strukturer
Det faktum att gener finns på kromosomer, verkar det som, inte motsvarar det faktum att människan bara har 23 par kromosomer och samtidigt tusentals olika egenskaper, som måste motsvara tusentals olika gener. Enbart tecken...
Spheroceridflugor (Diptera, Sphaeroceridae) i naturreservatet Kamyshanova Polyana
På Kamyshanova Polyana-reservatets territorium särskiljs följande typer av biotoper tydligt: skog, äng, olika vattennära, såväl som kantformationer ...
Bioteknikobjekt inom livsmedelsindustrin
Metabolism, eller metabolism, är den underliggande naturliga ordningen för omvandling av ämnen och energi i levande system, som syftar till deras bevarande och självreproduktion; helheten av alla kemiska reaktioner i kroppen ...
Cell koncept
XVII-talet 1665 - Den engelske fysikern R. Hooke beskriver i sitt arbete "Micrography" strukturen av korken, på de tunna sektionerna som han hittade korrekt placerade tomrum. Hooke kallade dessa tomrum "porer eller celler" ...
Mitokondriernas roll i apoptos
Fysiologi av cellulär excitation
· Bildandet av cellulär excitation beror just på transporten av joner. Bilipidskikt cellmembranet ogenomträngliga för joner (Na, K, Cl), jonkanaler är avsedda för deras transport in och ut ur cellen - speciella integrerade proteiner ...
Kemisk sammansättning celler
Alla levande organismer är kapabla att metabolisera med miljö... Processer pågår i cellerna biologisk syntes eller biosyntes...
- I kontakt med 0
- Google+ 0
- OK 0
- Facebook 0