No es ningún secreto que para que una persona mantenga la vida en nivel alto se necesita proteína, un tipo de material de construcción para los tejidos corporales; las proteínas contienen 20 aminoácidos, cuyos nombres es poco probable que le digan algo a un oficinista común. Cada persona, especialmente cuando se trata de mujeres, ha oído hablar al menos una vez sobre el colágeno y la queratina: estas son proteínas que son responsables de apariencia uñas, piel y cabello.
Aminoácidos: ¿qué es?
Los aminoácidos (o ácidos aminocarboxílicos; AMK; péptidos) son compuestos orgánicos, el 16% consisten en aminas - derivados orgánicos del amonio - lo que los distingue de los carbohidratos y los lípidos. Están involucrados en la biosíntesis de proteínas por parte del cuerpo: en el sistema digestivo, bajo la influencia de las enzimas, todas las proteínas que vienen con los alimentos se destruyen en AMK. En total, hay alrededor de 200 péptidos en la naturaleza, pero solo 20 aminoácidos básicos están involucrados en la construcción del cuerpo humano, que se dividen en intercambiables e insustituibles; a veces hay un tercer tipo: semireemplazable (reemplazable condicionalmente).

Aminoácidos no esenciales
Los aminoácidos no esenciales son aquellos que se consumen con los alimentos y se reproducen directamente en el cuerpo humano a partir de otras sustancias.
- La alanina es un monómero de compuestos biológicos y proteínas. Lleva a cabo una de las vías dominantes de la glucogénesis, es decir, se convierte en glucosa en el hígado y viceversa. Un participante muy activo en los procesos metabólicos en el cuerpo.
- La arginina es un AMA que se puede sintetizar en el cuerpo de un adulto, pero no se puede sintetizar en el cuerpo de un niño. Favorece la producción de hormonas de crecimiento y otras. El único portador de compuestos nitrogenados en el cuerpo. Ayuda a aumentar la masa muscular y reducir la grasa.
- La asparagina es un péptido implicado en el metabolismo del nitrógeno. Durante la reacción con la enzima asparaginasa, se separa el amoníaco y se convierte en ácido aspártico.
- Ácido aspártico: participa en la creación de inmunoglobulina, desactiva el amoníaco. Necesario para el mal funcionamiento de los sistemas nervioso y cardiovascular.
- Histidina: utilizada para prevenir y tratar enfermedades gastrointestinales; está marcando una diferencia positiva en la lucha contra el SIDA. Protege al organismo de los efectos nocivos del estrés.
- La glicina es un aminoácido neurotransmisor. Se utiliza como un sedante suave y antidepresivo. Potencia el efecto de algunos fármacos nootrópicos.
- Glutamina - en gran volumen Activador de procesos de reparación de tejidos.
- Ácido glutámico: tiene un efecto neurotransmisor y también estimula los procesos metabólicos en el sistema nervioso central.
- La prolina es uno de los componentes de casi todas las proteínas. Son especialmente ricos en elastina y colágeno, que son los responsables de la elasticidad de la piel.
- Serina - AMK que está contenida en las neuronas del cerebro y también contribuye a la liberación de grandes cantidades de energía. Es un derivado de la glicina.
- La tirosina es un componente de los tejidos animales y vegetales. Puede reproducirse a partir de fenilalanina por la acción de la enzima fenilalanina hidroxilasa; el proceso inverso no ocurre.
- La cisteína es uno de los componentes de la queratina, la cual es responsable de la firmeza y elasticidad del cabello, uñas y piel. También es un antioxidante. Puede estar hecho de serina.
Los aminoácidos que no se pueden sintetizar en el cuerpo son esenciales
Los aminoácidos esenciales son aquellos que no se pueden generar en el cuerpo humano y solo pueden provenir de los alimentos.
- La valina es un AMA que se encuentra en casi todas las proteínas. Aumenta la coordinación muscular y reduce la sensibilidad del cuerpo a los cambios de temperatura. Apoya la hormona serotonina en un nivel alto.
- La isoleucina es un anabólico natural que, en el proceso de oxidación, energiza el tejido muscular y cerebral.
- La leucina es un aminoácido que mejora el metabolismo. Es una especie de "constructor" de la estructura proteica.
- Estos tres AMC forman parte del llamado complejo BCAA, especialmente demandado entre los deportistas. Las sustancias de este grupo actúan como fuente para aumentar el volumen de la masa muscular, reducir la masa grasa y mantener una buena salud durante un esfuerzo físico especialmente intenso.
- La lisina es un péptido que acelera la regeneración de tejidos, la producción de hormonas, enzimas y anticuerpos. Responsable de la fuerza de los vasos sanguíneos, contenido en proteínas musculares y colágeno.
- Metionina: participa en la síntesis de colina, cuya falta puede provocar una mayor acumulación de grasa en el hígado.
- Treonina - da elasticidad y fuerza a los tendones. Tiene un efecto muy positivo sobre el músculo cardíaco y el esmalte dental.
- Triptófano: apoya el estado emocional, ya que se convierte en serotonina en el cuerpo. Indispensable para la depresión y otros trastornos psicológicos.
- Fenilalanina: mejora la apariencia de la piel, normalizando la pigmentación. Apoya el bienestar psicológico mejorando el estado de ánimo y aportando claridad al pensamiento.
Otros métodos para clasificar péptidos
Científicamente, los 20 aminoácidos esenciales se subdividen según la polaridad de su cadena lateral, es decir, los radicales. Así, se distinguen cuatro grupos: (pero sin carga), con carga positiva y con carga negativa.
No polares son: valina, alanina, leucina, isoleucina, metionina, glicina, triptófano, fenilalanina, prolina. A su vez, a la polar, teniendo carga negativa incluyen los ácidos aspártico y glutámico. Polar, que tiene una carga positiva, llamada arginina, histidina, lisina. Los aminoácidos con polaridad pero sin carga incluyen directamente cisteína, glutamina, serina, tirosina, treonina, asparagina.

20 aminoácidos: fórmulas (tabla)
Aminoácidos | Abreviatura | |
asparagina | ||
Ácido aspártico | ||
Histidina | ||
glutamina | ||
Ácido glutamico | ||
isoleucina | ||
metionina | ||
triptófano | ||
Fenilalanina | ||
Con base en esto, se puede notar que los 20 en la tabla anterior tienen carbono, hidrógeno, nitrógeno y oxígeno en su composición.
Aminoácidos: participación en la vida de la célula
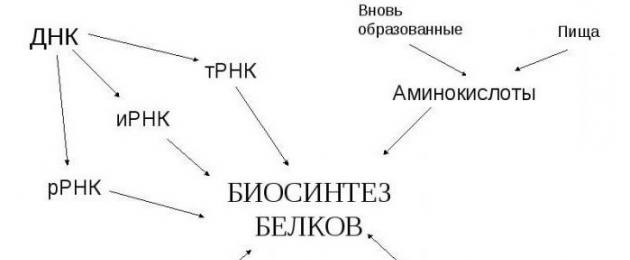
Los ácidos aminocarboxílicos están involucrados en la síntesis biológica de proteínas. La biosíntesis de proteínas es el proceso de modelado de una cadena polipeptídica ("poli" - muchos) a partir de residuos de aminoácidos. El proceso tiene lugar en el ribosoma, un orgánulo dentro de la célula que es directamente responsable de la biosíntesis.

La información se lee de una sección de la cadena de ADN de acuerdo con el principio de complementariedad (AT, CG), al crear m-RNA (matriz de ARN o i-RNA - ARN informativo - conceptos idénticamente iguales), se reemplaza la base nitrogenada timina por uracilo. Además, de acuerdo con el mismo principio, se crea una molécula de aminoácido transportadora en el sitio de síntesis. El T-RNA está codificado por tripletes (codones) (ejemplo: WAU), y si sabe qué bases nitrogenadas representa un triplete, puede averiguar qué aminoácido lleva.
Grupos de alimentos con mayor contenido de AUA
Los productos lácteos y los huevos contienen sustancias importantes como valina, leucina, isoleucina, arginina, triptófano, metionina y fenilalanina. Pescados, carnes blancas tienen un alto contenido en valina, leucina, isoleucina, histidina, metionina, lisina, fenilalanina, triptófano. Las legumbres, los granos y los cereales son ricos en valina, leucina, isoleucina, triptófano, metionina, treonina, metionina. Las nueces y varias semillas saturarán el cuerpo con treonina, isoleucina, lisina, arginina e histidina.
A continuación se muestra el contenido de aminoácidos de algunos alimentos.

La mayor cantidad de triptófano y metionina se encuentra en el queso duro, la lisina en la carne de conejo, la valina, la leucina, la isoleucina, la treonina y la fenilalanina en la soja. Al compilar una dieta basada en mantener un BUN normal, debe prestar atención a los calamares y los guisantes, y las papas y la leche de vaca pueden considerarse las más pobres en términos de contenido de péptidos.
Deficiencia de aminoácidos en el vegetarianismo
El hecho de que existan tales aminoácidos que se encuentran exclusivamente en productos animales es un mito. Además, los científicos han descubierto que el cuerpo humano absorbe mejor la proteína vegetal que la animal. Sin embargo, a la hora de elegir el vegetarianismo como estilo de vida, es muy importante seguir la dieta. El principal problema es que cien gramos de carne y la misma cantidad de frijoles contienen diferentes cantidades de AUA en términos porcentuales. En un primer momento, es necesario llevar registros del contenido de aminoácidos en los alimentos consumidos, luego esto debe alcanzar la automaticidad.
Cuantos aminoacidos se deben consumir al dia
V mundo moderno absolutamente todos los alimentos contienen los nutrientes necesarios para una persona, por lo que no debe preocuparse: los 20 aminoácidos de proteínas se suministran de manera segura con los alimentos, y esta cantidad es suficiente para una persona que lleva un estilo de vida normal y al menos cuida un poco su dieta.

La dieta del atleta debe estar saturada de proteínas, porque sin ellas es simplemente imposible desarrollar masa muscular. El ejercicio físico conduce a un consumo colosal de aminoácidos, por lo que los culturistas profesionales se ven obligados a tomar suplementos especiales. Con la construcción muscular intensiva, la cantidad de proteína puede alcanzar hasta cien gramos de proteína por día, pero tal dieta no es adecuada para el consumo diario. Cualquier suplemento alimenticio implica una instrucción con el contenido de diferentes AUA en una dosis, que debe leerse antes de usar el medicamento.
El efecto de los péptidos en la calidad de vida de una persona común.
La necesidad de proteínas está presente no solo entre los deportistas. Por ejemplo, las proteínas elastina, queratina, colágeno afectan la apariencia del cabello, la piel, las uñas, así como la flexibilidad y movilidad de las articulaciones. Una serie de aminoácidos afectan el cuerpo, mantienen el equilibrio de grasa en un nivel óptimo, proporcionan suficiente energía para La vida cotidiana. Después de todo, en el proceso de la vida, incluso con la forma de vida más pasiva, se gasta energía, al menos para respirar. Además, la actividad cognitiva también es imposible con la falta de ciertos péptidos; el mantenimiento del estado psicoemocional se lleva a cabo, entre otras cosas, a expensas de la AMC.
Aminoácidos y deportes
La dieta de los atletas profesionales implica una nutrición perfectamente equilibrada, que ayuda a mantener el tono muscular. Hacen la vida muy fácil, diseñados específicamente para aquellos deportistas que trabajan en ganar masa muscular.

Como se mencionó anteriormente, los aminoácidos son los principales componentes básicos de las proteínas necesarias para el crecimiento muscular. También son capaces de acelerar el metabolismo y quemar grasa, lo que también es importante para un hermoso alivio muscular. Cuando se hace ejercicio intenso, es necesario aumentar la ingesta de BUA porque aumentan la tasa de desarrollo muscular y reducen el dolor posterior al entrenamiento.
Los 20 aminoácidos de las proteínas se pueden consumir tanto como parte de los complejos aminocarboxílicos como de los alimentos. Si elige una dieta equilibrada, debe tener en cuenta absolutamente todos los gramos, lo cual es difícil de implementar con una gran carga de trabajo del día.
Qué le sucede al cuerpo humano cuando hay una falta o un exceso de aminoácidos
Los principales síntomas de la deficiencia de aminoácidos son: mala salud, falta de apetito, uñas quebradizas, aumento de la fatiga. Incluso con la falta de un BUN, hay una gran cantidad de efectos secundarios desagradables que afectan significativamente el bienestar y la productividad.
La sobresaturación con aminoácidos puede provocar alteraciones en el funcionamiento de los sistemas cardiovascular y nervioso, lo que, a su vez, no es menos peligroso. A su vez, pueden aparecer síntomas similares a una intoxicación alimentaria, lo que tampoco conlleva nada agradable.
En todo lo que necesita saber cuándo parar, por lo que mantener un estilo de vida saludable no debería conducir a una sobreabundancia de ciertas sustancias "útiles" en el cuerpo. Como escribió el clásico, “lo mejor es enemigo de lo bueno”.
En el artículo, examinamos las fórmulas y los nombres de los 20 aminoácidos, la tabla del contenido de los principales AMK en los productos se muestra arriba.
La bioquímica combina la biología y la química. Esta ciencia se ocupa del estudio de las vías metabólicas (transformaciones químicas) en los organismos vivos a nivel celular. Además de ser el estudio de las rutas metabólicas en plantas y microorganismos, la bioquímica es ciencia experimental, para lo cual se requiere equipo especial. Esta vasta ciencia se basa en una serie de conceptos e ideas básicos que se estudian al comienzo del curso de bioquímica.
Pasos
Parte 1
Conoce los conceptos básicos- Aprende cinco grupos de aminoácidos, cuatro ácidos en cada grupo.
- Recuerda las propiedades importantes de los aminoácidos, como la carga y la polaridad.
- Una y otra vez dibuja la estructura de los aminoácidos hasta que se deposite en tu memoria.
-
Familiarízate con la estructura de las proteínas. Las proteínas están formadas por cadenas de aminoácidos. Para conocer los fundamentos de la bioquímica, es necesario reconocer los distintos niveles de estructura de las proteínas y ser capaz de representar los más importantes (hélices alfa y láminas beta). Hay cuatro niveles de estructura proteica:
- La estructura primaria es una disposición lineal de aminoácidos.
- La estructura secundaria corresponde a secciones de la proteína en forma de hélices alfa y láminas beta.
- Estructura terciaria- Esta es la estructura tridimensional de la molécula de proteína, que se debe a la interacción de los aminoácidos. Esta es la forma fisiológica de la proteína. La estructura terciaria de muchas proteínas aún se desconoce.
- La estructura cuaternaria resulta de la interacción de varias proteínas que forman una molécula de proteína más grande.
-
Aprende sobre el nivel de pH. El nivel de pH de una solución caracteriza su acidez. Indica la cantidad de iones de hidrógeno y de iones de hidróxido presentes en la solución. Las soluciones ácidas contienen más iones de hidrógeno y relativamente pocos iones de hidróxido. Por el contrario, los iones de hidróxido predominan en soluciones alcalinas.
- Los ácidos actúan como donantes de iones de hidrógeno (H+).
- Los álcalis son aceptores de iones de hidrógeno (H+).
-
Aprende a determinar el pKa de una solución. La constante de disociación de un ácido, Ka, indica con qué facilidad un ácido cede iones de hidrógeno en una solución dada. Esta constante se define como Ka = /. Para la mayoría de las soluciones, K a se puede encontrar en tablas en libros de referencia o en Internet. El valor pK a se define como el logaritmo decimal negativo de la constante K a .
- ácidos fuertes tienen valores de pKa muy bajos.
-
Aprenda a encontrar el pH a partir de pKa usando la ecuación de Henderson-Hasselbach. Esta ecuación se utiliza para preparar soluciones tampón en el laboratorio. La ecuación de Henderson-Hasselbach se escribe de la siguiente manera: pH = pK a + lg [base]/[ácido]. El valor pKa de una solución es igual al nivel de pH de esta solución si las concentraciones de ácido y base son las mismas.
Aprende sobre los enlaces químicos iónicos y covalentes. Un enlace iónico entre átomos ocurre cuando uno o más electrones se mueven de un átomo a otro. Como resultado, se forman iones positivos y negativos, que se atraen entre sí. En un enlace covalente, los átomos intercambian pares de electrones.
Aprende sobre las enzimas. Las enzimas son proteínas que juegan un papel importante en el cuerpo: catalizan (aceleran) las reacciones bioquímicas. Casi todas las reacciones bioquímicas del cuerpo son aceleradas por una determinada enzima, por lo que el estudio de la acción catalítica de las enzimas es la tarea más importante de la bioquímica. Los mecanismos catalíticos se estudian principalmente desde el punto de vista de la cinética.
- La inhibición enzimática se utiliza en farmacología para tratar muchos tipos de enfermedades.
Parte 2
Recuerda las rutas metabólicas-
Infórmese sobre las vías metabólicas y los gráficos relacionados con el estudio. Hay muchas vías metabólicas importantes para recordar al estudiar bioquímica. En particular, estas vías incluyen: la glucólisis, la fosforilación oxidativa, el ciclo de los ácidos tricarboxílicos (ciclo de Krebs), la cadena respiratoria de transporte de electrones, la fotosíntesis.
- Leer descripciones de rutas metabólicas y estudiar sus representaciones en diagramas.
- Es posible que durante el examen te pidan que dibujes un esquema completo de una u otra vía metabólica.
-
Aprende un camino a la vez. Si intenta aprender todas las rutas metabólicas al mismo tiempo, se confundirá y no podrá recordar ninguna de ellas correctamente. Concéntrate en un camino y dedícale unos días antes de pasar al siguiente.
- Una vez que memorices un camino, trata de no olvidarlo. Dibuja este camino a menudo para refrescar tu memoria.
-
Dibuja el camino principal. Comience por aprender la vía metabólica principal. Algunas vías son ciclos repetitivos (ciclo del ácido tricarboxílico), otras son procesos lineales (glucólisis). Para empezar, memoriza la forma del camino, dónde comienza, qué sustancias se descomponen y cuáles se sintetizan.
- Al principio de cada ciclo hay moléculas de partida, como el dinucleótido de nicotinamida y adenina, el difosfato de adenosina (ADP) o la glucosa, y productos finales, como el trifosfato de adenosina o el glucógeno. En primer lugar, recuerde los materiales de partida y los productos finales.
-
Examinar coenzimas y metabolitos. Ahora echa un vistazo a este camino con más detalle. Los metabolitos son productos intermedios que se forman durante el proceso, se utilizan en reacciones posteriores. También hay coenzimas que hacen posible una reacción o la aceleran.
-
Anote las enzimas necesarias. El paso final en el estudio de la ruta metabólica es agregarle las enzimas necesarias para que se lleven a cabo las reacciones. Esta memorización paso a paso del camino te facilitará la tarea. Completará su estudio de la ruta metabólica después de memorizar los nombres de las enzimas relevantes.
- Después de eso, puede anotar fácilmente todas las proteínas, metabolitos y moléculas que están involucradas en esta vía metabólica.
-
Repite los caminos que has aprendido regularmente. Este tipo de información debe actualizarse semanalmente o la olvidará. Repita una ruta metabólica todos los días. Al final de la semana, repetirá todos los caminos y podrá comenzar de nuevo la próxima semana.
- Cuando el tiempo es correcto trabajo de control o un examen, no tienes que memorizar frenéticamente las rutas metabólicas porque ya las conoces.
Recuerda la estructura de los aminoácidos. Los aminoácidos son los componentes básicos que forman todas las proteínas. Al estudiar bioquímica, es necesario recordar la estructura y las propiedades de los 20 aminoácidos. Aprenda sus designaciones de una y tres letras para que pueda reconocerlas fácilmente más adelante.
Ksyu
Entonces, ¿es esto una broma? ¿Cómo aprender bioquímica?
administración
Bueno, ¿cómo, cómo? Enseñar. Qué tipo de bromas puede haber aquí. Aunque, de que hablo... Más de la mitad no sabe leer, pero hablo de bioquímica...
ejemplo sencillo
El formulario de registro en el sitio dice:
Apellido, iniciales:
Es decir, algo como calabaza II Apellido e iniciales.
Dos de tres los estudiantes llenan solo apellido. En "años de cosecha" - tres de cuatro.
¿Eso es lo que es? ¿Descuido? ¿Falta de vocabulario? ¿Indiferencia?
Entonces, el tema también se enseña: el maestro descargó las notas de la lección, se desplazó en diagonal, como lo preparó. Oh bien...
administración
A medida que se acerca la sesión, hay un aumento similar a una avalancha en las lecturas de este material.
Gavrilenko Alena Valerievna
Gran artículo sobre la ciencia joven del futuro, gracias. Y en qué sitios puedes encontrar animaciones de biología molecular, videos "bioquímicos", algo así como en el canal Eto Works, en ruso. ¿Y hay conferencias de audio para descargar gratis en Internet en ruso o a través de qué sitio es mejor pedirlas para comprarlas? Y, si no es difícil, dígame los servidores en línea para realizar cambios en los archivos PDB. Gracias.
administración
¿En ruso? se puede ver en un solo portal educativo, aunque ahí, francamente hablando, el nivel de la escuela. A menudo la información está desactualizada, con errores. Lo más probable es que tenga que traducir por su cuenta: editores de gif, editores de video. Es posible que puedas dibujar o dispararte a ti mismo (solo). Vengo del hecho de que cada video o animación que se puede encontrar en la web fue hecho con un propósito específico.Gavrilenko Alena Valerievna
Y en qué sitios puedes encontrar animaciones de biología molecular, videos "bioquímicos", algo así como en el canal Eto Works, en ruso.
Audio conferencias? por bioquimica??? Nunca me ha interesado esta pregunta... No tengo idea de cómo dar, por ejemplo, bioquímica estructural exclusivamente de oído. Quiralidad, estereoisomerismo para decirle a los estudiantes que tienen los ojos vendados. Incluso con presentaciones / gráficos, no entienden de inmediato de qué se trata ...Gavrilenko Alena Valerievna
¿Y hay conferencias de audio para descargar gratis en Internet en ruso o a través de qué sitio es mejor pedirlas para comprarlas?
En cuanto a la descarga gratuita... En la actualidad, teniendo en cuenta la monetización de todo y de todos, así como teniendo en cuenta el Copyright For Any Junk - gratis fuentes calidad no hay contenido. Si algo existe de repente, lo más probable es que sea un pirata franco.
Con respecto a la compra, ¿quizás debería prestar atención a las conferencias en video? Ver centros la educación a distancia en las universidades, buscar canales en YouTube. Aunque allí también todo es triste... En el canal de la Universidad Estatal de Moscú, por ejemplo, hay hasta 7 videos de la Facultad de Química y 10 videos de la Facultad de Biología. No hay conjuntos completos de conferencias, aunque sé con certeza que las conferencias del prof. Milekyan, por ejemplo. Spirin escribió. ¿Necesita ponerse en contacto con el centro de aprendizaje a distancia para averiguar si se ha digitalizado? Si es así, cómo obtener/comprar/intercambiar.
http://deposit.rcsb.org/ - depósitoGavrilenko Alena Valerievna
por favor dígame servidores en línea para hacer cambios en los archivos PDB.
http://deposit.rcsb.org/depoinfo/depofaq.html - Preguntas frecuentes sobre la colocación.
Hay todas las instrucciones: cómo verificar, cómo formatear, qué y cómo empacar archivos.
alyona
Quiero convertirme en un bisonte en el acoplamiento de proteínas, no importa cuán ridículo suene con mi conocimiento nulo de química y física. Pretendiendo enseñar física de proteínas de Finkelstein y teoría y práctica de modelado molecular por Hölte, Zippl, Ronjan, Volkers, parecía que esto podría ayudarme. ¿En qué literatura puedo encontrar algún sentido en mi situación y qué programas gratuitos en una PC puedo descargar para el acoplamiento de proteínas?
administración
Servidor NCBI, por supuesto. buscar la palabra clave: acoplamiento de proteínas. Allí, en la búsqueda de artículos, encontrarás todas las novedades sobre el software utilizado, algoritmos, principios, etc. En cualquier caso, la búsqueda es mejor comenzar desde allí.alyona
¿En qué literatura puedo encontrar algún sentido en mi situación?
Habrá un problema con el software libre... Dado que la predicción de la estructura es un lugar potencial de "pan" - el diseño de fármacos, por ejemplo, el software libre tendrá que buscarse intensamente...alyona
¿Y qué programas gratuitos descargar en una PC para el acoplamiento de proteínas?
Aconsejaría usar software de servidor para empezar. El acoplamiento, de hecho, es la predicción de una estructura tridimensional y opciones para su empaquetamiento con moléculas vecinas (dominios). Los cálculos son muy "glotones" y exigen recursos de la computadora; de alguna manera, no estoy contento con la computadora constantemente colgada y el cálculo, que dura una semana.
De nuevo, en el oeste mundo cientifico no todos los rednecks todavía, y algunos programas se pueden obtener de forma gratuita bajo una licencia académica: http://www.russelllab.org/cgi-bin/tools/interprets.pl
Sí, mire también hacia BioLinux, un buen ensamblaje para bioinformática, con una licencia gratuita.
Ruslán
Hola, me interesó un mapa de rutas metabólicas (el indicado en la descripción). No me digas donde se puede descargar? PD No encontré tal oportunidad en el sitio indicado en la descripción. Gracias por adelantado.
administración
En ningún lugar. No es posible descargar este mapa en un archivo (pieza completa).Ruslán
No me digas donde se puede descargar?
en forma electrónica, se encuentra en el sitio especificado, es decir, en forma de mapa:
Versión electrónica
Tras el gran éxito de los dos carteles durante más de cuatro décadas y de la versión electrónica alojada en ExPASy desde 1994, Roche ha creado una nueva versión electrónica de Biochemical Pathways.
Por sí mismo. Ganan dinero con esto, y mucho. Puede usar su sitio, aumentando constantemente el tráfico hacia él, o puede solicitar una tarjeta ya impresa, un póster pesado como este:Ruslán
No encontré tal oportunidad en el sitio indicado en la descripción.
copia impresa
Se han distribuido más de 700 000 copias impresas de los gráficos murales a investigadores y estudiantes de medicina y ciencias de la vida de todo el mundo. el formulario de pedido.calabaza II
Los productos químicos que contienen los componentes estructurales de un ácido carboxílico y una molécula de amina se denominan aminoácidos. Este es el nombre general de un grupo de compuestos orgánicos que contienen una cadena hidrocarbonada, un grupo carboxilo (-COOH) y un grupo amino (-NH2). Sus precursores son los ácidos carboxílicos, y las moléculas en las que el hidrógeno del primer átomo de carbono se reemplaza por un grupo amino se denominan alfa-aminoácidos.
Solo 20 aminoácidos son valiosos para las reacciones enzimáticas de biosíntesis que ocurren en el cuerpo de todos los seres vivos. Estas sustancias se denominan aminoácidos estándar. También hay aminoácidos no estándar que se incluyen en algunas moléculas de proteínas especiales. No se encuentran en todas partes, aunque cumplen una función importante en la vida silvestre. Probablemente, los radicales de estos ácidos se modifican después de la biosíntesis.
Información general y lista de sustancias
Dos grandes grupos aminoácidos que fueron aislados debido a los patrones de su presencia en la naturaleza. En particular, hay 20 aminoácidos estándar y 26 aminoácidos no estándar. Los primeros se encuentran en la composición de las proteínas de cualquier organismo vivo, mientras que los segundos son específicos de organismos vivos individuales.
20 aminoácidos estándar se dividen en 2 tipos dependiendo de la capacidad de sintetizarse en cuerpo humano. Estos son reemplazables, los que en las células humanas son capaces de formarse a partir de precursores, e insustituibles, para cuya síntesis no existen sistemas enzimáticos o sustrato. Los aminoácidos no esenciales pueden no estar presentes en los alimentos, ya que su cuerpo puede sintetizarlos, reponiendo su cantidad si es necesario. El cuerpo no puede obtener los aminoácidos esenciales por sí solos y, por lo tanto, debe obtenerlos de los alimentos.
Los bioquímicos han determinado los nombres de los aminoácidos del grupo de los esenciales. Hay 8 conocidos en total:
- metionina;
- treonina;
- isoleucina;
- leucina;
- fenilalanina;
- triptófano;
- valina;
- lisina;
- la histidina también se incluye a menudo aquí.
Son sustancias con una estructura diferente del radical hidrocarbonado, pero siempre con la presencia de un grupo carboxilo y un grupo amino en el átomo alfa C.
Hay 11 sustancias en el grupo de aminoácidos no esenciales:
- alanina;
- glicina;
- arginina;
- asparagina;
- ácido aspártico;
- cisteína;
- ácido glutamico;
- glutamina;
- prolina;
- serina;
- tirosina.
Básicamente, su estructura química es más sencilla que la de los esenciales, por lo que su síntesis es más fácil para el organismo. La mayoría de los aminoácidos esenciales no se pueden obtener únicamente por la falta de un sustrato, es decir, una molécula precursora, a través de la reacción de transaminación.
Glicina, alanina, valina
En la biosíntesis de moléculas de proteínas, las más utilizadas son la glicina, la valina y la alanina (la fórmula de cada sustancia se muestra en la siguiente figura). Estos aminoácidos son los más simples. Estructura química. La sustancia glicina es la más simple de la clase de aminoácidos, es decir, además del átomo de carbono alfa, el compuesto no tiene radicales. Sin embargo, incluso la molécula más simple en estructura juega un papel importante para asegurar la vida. En particular, el anillo de porfirina de la hemoglobina y las bases de purina se sintetizan a partir de la glicina. El anillo de pórfido es una región proteica de la hemoglobina, diseñada para contener átomos de hierro en la composición de una sustancia integral.
La glicina interviene en el aseguramiento de la actividad vital del cerebro, actuando como mediador inhibitorio del sistema nervioso central. Esto significa que él está en más participa en el trabajo de la corteza cerebral, su tejido organizado de forma más compleja. Más importante aún, la glicina es un sustrato para la síntesis de bases de purina necesarias para la formación de nucleótidos que codifican información hereditaria. Además, la glicina sirve como fuente para la síntesis de otros 20 aminoácidos, mientras que ella misma puede formarse a partir de la serina.

El aminoácido alanina tiene una fórmula un poco más compleja que la glicina, ya que tiene un radical metilo reemplazado por un átomo de hidrógeno en el átomo de carbono alfa de la sustancia. Al mismo tiempo, la alanina también sigue siendo una de las moléculas más frecuentemente involucradas en los procesos de biosíntesis de proteínas. Es parte de cualquier proteína en la vida silvestre.
Incapaz de ser sintetizada en el cuerpo humano, la valina es un aminoácido con una cadena hidrocarbonada ramificada que consta de tres átomos de carbono. El radical isopropilo le da más peso a la molécula, pero debido a esto, es imposible encontrar un sustrato para la biosíntesis en las células de los órganos humanos. Por lo tanto, la valina debe suministrarse con alimentos. Está presente predominantemente en las proteínas estructurales de los músculos.
Los resultados de los estudios confirman que la valina es necesaria para el funcionamiento del sistema central sistema nervioso. En particular, debido a su capacidad para restaurar la vaina de mielina de las fibras nerviosas, puede usarse como ayuda en el tratamiento de la esclerosis múltiple, la adicción a las drogas y la depresión. Se encuentra en grandes cantidades en productos cárnicos, arroz, guisantes secos.
Tirosina, histidina, triptófano
En el cuerpo, la tirosina se puede sintetizar a partir de la fenilalanina, aunque se suministra en grandes cantidades con los productos lácteos, principalmente con requesón y quesos. Incluido en la composición de caseína - proteína animal, contenida en exceso en requesón y productos de queso. La importancia clave de la tirosina es que su molécula se convierte en sustrato para la síntesis de catecolaminas. Estos son adrenalina, norepinefrina, dopamina, mediadores del sistema humoral de regulación de las funciones corporales. La tirosina puede penetrar rápidamente la barrera hematoencefálica, donde rápidamente se convierte en dopamina. La molécula de tirosina participa en la síntesis de melanina, aportando pigmentación a la piel, el cabello y el iris del ojo.
El aminoácido histidina forma parte de las proteínas estructurales y enzimáticas del organismo, es sustrato para la síntesis de histamina. Este último regula la secreción gástrica, participa en reacciones inmunes, regula la curación de lesiones. La histidina es un aminoácido esencial y el cuerpo repone sus reservas solo a partir de los alimentos.

El triptófano tampoco puede ser sintetizado por el cuerpo debido a la complejidad de su cadena hidrocarbonada. Forma parte de las proteínas y es sustrato para la síntesis de la serotonina. Este último es un mediador del sistema nervioso, diseñado para regular los ciclos de vigilia y sueño. Triptófano y tirosina: los neurofisiólogos deben recordar estos nombres de aminoácidos, ya que a partir de ellos se sintetizan los principales mediadores del sistema límbico (serotonina y dopamina), que aseguran la presencia de emociones. Al mismo tiempo, no existe una forma molecular que asegure la acumulación de aminoácidos esenciales en los tejidos, por lo que deben estar presentes en los alimentos todos los días. Los alimentos proteicos en la cantidad de 70 gramos por día satisfacen plenamente estas necesidades del cuerpo.
Fenilalanina, leucina e isoleucina
La fenilalanina se destaca por el hecho de que el aminoácido tirosina se sintetiza a partir de ella cuando es deficiente. La propia fenilalanina es componente estructural todas las proteínas en la naturaleza. Es el precursor metabólico del neurotransmisor fenetilamina, que proporciona concentración mental, elevación del estado de ánimo y psicoestimulación. En la Federación Rusa, en una concentración superior al 15%, está prohibida la circulación de esta sustancia. El efecto de la feniletilamina es similar al de la anfetamina, pero la primera no tiene un efecto dañino en el cuerpo y difiere solo en el desarrollo de la dependencia mental.
Una de las principales sustancias del grupo de los aminoácidos es la leucina, a partir de la cual se sintetizan las cadenas peptídicas de cualquier proteína humana, incluidas las enzimas. El compuesto, utilizado en su forma pura, es capaz de regular las funciones del hígado, acelerar la regeneración de sus células y rejuvenecer el cuerpo. Por lo tanto, la leucina es un aminoácido que está disponible en forma de fármaco. Es altamente eficaz en el tratamiento auxiliar de la cirrosis hepática, anemia, leucemia. La leucina es un aminoácido que facilita enormemente la rehabilitación de los pacientes después de la quimioterapia.

La isoleucina, como la leucina, no puede ser sintetizada por el cuerpo por sí sola y pertenece al grupo de indispensables. Sin embargo, esta sustancia no es medicamento porque el cuerpo tiene poca necesidad de ella. Básicamente, solo uno de sus estereoisómeros (2S,3S)-2-amino-3-metilpentanoico está involucrado en la biosíntesis.
Prolina, serina, cisteína
La prolina es un aminoácido con un radical hidrocarbonado cíclico. Su valor principal está en presencia del grupo cetona de la cadena, por lo que la sustancia se usa activamente en la síntesis. proteínas estructurales. La reducción de la cetona heterociclo a un grupo hidroxilo con la formación de hidroxiprolina forma múltiples enlaces de hidrógeno entre las cadenas de colágeno. Como resultado, las hebras de esta proteína se entrelazan y proporcionan una fuerte estructura intermolecular.
La prolina es un aminoácido que proporciona resistencia mecánica a los tejidos humanos y su esqueleto. La mayoría de las veces se encuentra en el colágeno, que forma parte de los huesos, cartílagos y tejido conectivo. Al igual que la prolina, la cisteína es el aminoácido del que proteína estructural. Sin embargo, no se trata de colágeno, sino de un grupo de sustancias llamadas alfa-queratinas. Forman el estrato córneo de la piel, las uñas, forman parte de las escamas del cabello.

La sustancia serina es un aminoácido que existe como isómeros ópticos L y D. Es una sustancia intercambiable sintetizada a partir de fosfoglicerato. La serina se puede formar durante una reacción enzimática a partir de la glicina. Esta interacción es reversible y, por lo tanto, la glicina se puede formar a partir de la serina. El principal valor de este último es que las proteínas enzimáticas, o más bien sus centros activos, se sintetizan a partir de la serina. La serina está ampliamente presente en las proteínas estructurales.
Arginina, metionina, treonina
Los bioquímicos han determinado que el consumo excesivo de arginina provoca el desarrollo de la enfermedad de Alzheimer. Sin embargo, además del valor negativo, la sustancia también tiene funciones vitales para la reproducción. En particular, debido a la presencia del grupo guanidina, que existe en la célula en forma catiónica, el compuesto puede formar una gran cantidad de enlaces de hidrógeno intermoleculares. Debido a esto, la arginina en forma de zwitterión adquiere la capacidad de unirse a las regiones de fosfato de las moléculas de ADN. El resultado de la interacción es la formación de muchas nucleoproteínas, la forma de empaquetamiento del ADN. La arginina en el curso de los cambios en el pH de la matriz nuclear de la célula puede desprenderse de la nucleoproteína, proporcionando el desenrollado de la cadena de ADN y el comienzo de la traducción para la biosíntesis de proteínas.
El aminoácido metionina contiene un átomo de azufre en su estructura, por lo que una sustancia pura en forma cristalina tiene un desagradable olor a podrido debido a la liberación de sulfuro de hidrógeno. En el cuerpo humano, la metionina realiza una función regeneradora, favoreciendo la cicatrización de las membranas celulares del hígado. Por lo tanto, se produce en forma de preparación de aminoácidos. A partir de la metionina también se sintetiza un segundo fármaco, destinado al diagnóstico de tumores. Se sintetiza reemplazando un átomo de carbono con su isótopo C11. De esta forma, se acumula activamente en las células tumorales, lo que permite determinar el tamaño de los tumores cerebrales.
A diferencia de los aminoácidos anteriores, la treonina es de menor importancia: los aminoácidos no se sintetizan a partir de ella y su contenido en los tejidos es bajo. El principal valor de la treonina es su inclusión en la composición de las proteínas. Este aminoácido no tiene funciones específicas.
Asparagina, lisina, glutamina
La asparagina es un aminoácido no esencial común presente como el isómero L de sabor dulce y el isómero D amargo. Las proteínas del cuerpo se forman a partir de la asparagina y el oxaloacetato se sintetiza por gluconeogénesis. Esta sustancia es capaz de oxidarse en el ciclo de los ácidos tricarboxílicos y proporcionar energía. Esto significa que además de la función estructural, la asparagina también realiza una función energética.
Incapaz de ser sintetizada en el cuerpo humano, la lisina es un aminoácido con propiedades alcalinas. A partir de él, se sintetizan principalmente proteínas inmunitarias, enzimas y hormonas. Al mismo tiempo, la lisina es un aminoácido que manifiesta de forma independiente agentes antivirales contra el virus del herpes. Sin embargo, la sustancia no se usa como droga.

El aminoácido glutamina está presente en la sangre en concentraciones muy por encima de otros aminoácidos. Desempeña un papel importante en los mecanismos bioquímicos del metabolismo del nitrógeno y la excreción de metabolitos, participa en la síntesis de ácidos nucleicos, enzimas, hormonas y es capaz de fortalecer el sistema inmunitario, aunque no se utiliza como fármaco. Pero la glutamina se usa ampliamente entre los atletas, ya que ayuda a recuperarse del entrenamiento, elimina los metabolitos de nitrógeno y butirato de la sangre y los músculos. Este mecanismo para acelerar la recuperación de un atleta no se considera artificial y no se reconoce correctamente como dopaje. Además, no existen métodos de laboratorio para condenar a los atletas por dicho dopaje. La glutamina también está presente en cantidades significativas en los alimentos.
Ácido aspártico y glutámico
Los aminoácidos aspártico y glutamina son extremadamente valiosos para el cuerpo humano debido a sus propiedades que activan los neurotransmisores. Aceleran la transferencia de información entre neuronas, asegurando el mantenimiento de las estructuras cerebrales que se encuentran debajo de la corteza. En tales estructuras, la confiabilidad y la constancia son importantes, porque estos centros regulan la respiración y la circulación sanguínea. Por lo tanto, hay una gran cantidad de aminoácidos de aspártico y glutamina en la sangre. La fórmula estructural espacial de los aminoácidos se muestra en la siguiente figura.
El ácido aspártico interviene en la síntesis de la urea, eliminando el amoníaco del cerebro. Es una sustancia importante para mantener una alta tasa de reproducción y renovación de las células sanguíneas. Por supuesto, en la leucemia, este mecanismo es dañino y, por lo tanto, para lograr la remisión, se usan preparaciones enzimáticas que destruyen el aminoácido aspártico.
Una cuarta parte de todos los aminoácidos en el cuerpo es ácido glutámico. Este es un neurotransmisor de los receptores postsinápticos, necesarios para la transmisión sináptica de un impulso entre los procesos de las neuronas. Sin embargo, el ácido glutámico también se caracteriza por una forma extrasináptica de transmitir información: la neurotransmisión volumétrica. Este método subyace a la memoria y es un misterio neurofisiológico, porque aún no se ha aclarado qué receptores determinan la cantidad de glutamato fuera de la célula y fuera de las sinapsis. Sin embargo, se supone que es la cantidad de sustancia fuera de la sinapsis lo que es importante para la neurotransmisión masiva.
Estructura química
Todos los aminoácidos no estándar y los 20 estándar tienen un plan estructural común. Incluye una cadena hidrocarbonada cíclica o alifática con o sin radicales, un grupo amino en el átomo de carbono alfa y un grupo carboxilo. La cadena de hidrocarburo puede ser cualquiera, por lo que la sustancia tiene la reactividad de los aminoácidos, la ubicación de los radicales principales es importante.

El grupo amino y el grupo carboxilo deben estar unidos al primer átomo de carbono de la cadena. Según la nomenclatura aceptada en bioquímica, se denomina átomo alfa. Esto es importante para la formación de un grupo peptídico - el más importante enlace químico que hace que las proteínas existan. Desde el punto de vista de la química biológica, la vida es el modo de existencia de las moléculas de proteína. El papel principal de los aminoácidos es la formación enlace peptídico. La fórmula estructural general de los aminoácidos se presenta en el artículo.
Propiedades físicas
A pesar de la estructura similar de la cadena hidrocarbonada, los aminoácidos difieren significativamente de las propiedades físicas de los ácidos carboxílicos. A temperatura ambiente, son sustancias cristalinas hidrófilas, fácilmente solubles en agua. En un solvente orgánico, debido a la disociación del grupo carboxilo y la eliminación de un protón, los aminoácidos se disuelven mal, formando mezclas de sustancias, pero no verdaderas soluciones. Muchos aminoácidos tienen un sabor dulce, mientras que los ácidos carboxílicos son ácidos.
Especificado propiedades físicas debido a la presencia de dos grupos químicos funcionales, por lo que la sustancia en el agua se comporta como una sal disuelta. Bajo la acción de las moléculas de agua, se separa un protón del grupo carboxilo, cuyo aceptor es el grupo amino. Debido al cambio en la densidad electrónica de la molécula y la ausencia de protones que se mueven libremente pH (índice de acidez), la solución permanece bastante estable cuando se agregan ácidos o álcalis con constantes de disociación altas. Esto significa que los aminoácidos pueden formar sistemas amortiguadores débiles, manteniendo la homeostasis del cuerpo.
Es importante que el módulo de carga de la molécula de aminoácido disociada sea cero, ya que el átomo de nitrógeno acepta el protón separado del grupo hidroxilo. Sin embargo, se forma una carga positiva en el nitrógeno de la solución y una carga negativa en el grupo carboxilo. La capacidad de disociarse depende directamente de la acidez y, por lo tanto, existe un punto isoeléctrico para las soluciones de aminoácidos. Este es el pH (índice de acidez) en el que la mayor cantidad de moléculas tienen carga cero. En este estado, están inmóviles en un campo eléctrico y no conducen corriente.
Probablemente, valga la pena comenzar con el hecho de que el cuerpo humano está compuesto aproximadamente en una cuarta parte (o un poco menos) por proteínas, es decir, proteínas. Los niños los necesitan para su crecimiento y desarrollo. Podemos decir que las proteínas son el marco, la base de nuestro cuerpo.
Al mismo tiempo, cada proteína realiza su propia cantidad de trabajo estrictamente definida: por ejemplo, la hemoglobina es responsable de enriquecer el cuerpo del bebé con oxígeno, miosina y actina; para el desarrollo y la contracción de los músculos, la insulina afecta el metabolismo, la queratina es un componente importante del cabello y las uñas, y es impensable sin la formación de colágeno de huesos, piel y tendones. Gracias al apoyo de proteínas, el sistema inmunológico del niño resiste las infecciones y su psique se enfrenta fácilmente al estrés.
Son vegetales y animales y entran al cuerpo durante las comidas. Cuando un bebé come un producto en particular, las proteínas que contiene ingresan al tracto gastrointestinal y se descomponen en aminoácidos. Y luego forman sus propias proteínas humanas: "material de construcción" para el desarrollo y la renovación constante de órganos y tejidos. Los aminoácidos también son responsables de garantizar que este proceso sea continuo: el crecimiento es estable, la renovación celular es ininterrumpida, el desarrollo del pensamiento es constante.
Afortunadamente, las mamás no tienen que buscar alimentos especiales o raros para proporcionar a sus pequeños todas las proteínas que necesitan: están presentes en la mayoría de las comidas que tradicionalmente se dan a los bebés. Así, el bebé recibe proteínas vegetales, en particular, de las verduras, frutas, cereales y legumbres, y las animales de la carne, los huevos, el pescado y la leche. Ambos son importantes para su salud.
¿Qué te gustaría comer?
Se sabe que un conjunto completo de aminoácidos esenciales está presente en las proteínas de los productos animales: huevos y leche, así como en las proteínas de soja. Mientras que en los alimentos vegetales, los aminoácidos se distribuyen de forma algo desigual, como si estuvieran “esparcidos” entre diferentes productos: unos están presentes en las verduras, otros en los frutos secos, otros en las algas y un cuarto en el sésamo.
Por lo tanto, no se puede decir que un bebé adulto, en cuya dieta estarán presentes los productos de origen animal enumerados, no podrá cambiar a una dieta vegetariana sin dañar la salud. Sin embargo, dado que la mayoría de los padres no tienen conocimientos profesionales en esta área, contactar a un pediatra, e idealmente a un dietista, será un paso responsable. Solo un especialista en fuerza puede calcular la dieta de un hombre fuerte, incluidos los productos vegetales que pueden satisfacer la necesidad de aminoácidos de un cuerpo en crecimiento, en las proporciones correctas, teniendo en cuenta la edad, el estado de salud y el desarrollo del niño.
Habiendo recibido tal asesoramiento profesional, en el futuro, mamá y papá podrán seguir de forma independiente las recomendaciones de un especialista y agregar ciertos platos. Es bastante posible hacer esto, teniendo suficiente información sobre cada producto requerido, especialmente porque hay información más que suficiente en la World Wide Web. Por ejemplo, se sabe que la cantidad de aminoácidos esenciales contenidos en las proteínas de los frutos secos prácticamente los acerca al estándar: la llamada "proteína ideal" de un huevo de gallina. Sin embargo, debe estar preparado para buscar productos que son necesarios para una dieta completa, pero al mismo tiempo, bastante raros para nuestra franja de productos, por ejemplo, leche de almendras o espirulina.
Al considerar la idea de transferir a un niño a una dieta vegetariana, los padres también deben tener en cuenta la información de que, a pesar del valor nutricional comprobado, las proteínas vegetales, con la excepción de la soya, todavía son absorbidas por el cuerpo solo en un 60 por ciento. , mientras que los animales - los 90.
Sea como fuere, la parte principal de los alimentos ricos en proteína vegetal aparecerán en la dieta del bebé un poco más tarde (a excepción de la soja, que se incluye, en particular, en algunas fórmulas infantiles, y las verduras).
Absolutamente insustituible
Si hablamos de migajas hasta los tres años, para satisfacer la necesidad de aminoácidos de su cuerpo, el menú diario debe diseñarse de tal manera que el niño reciba al menos 53 gramos de proteína con la comida, y la mayor parte - 37 gramos - debe ser de origen animal, y solo 16 gramos - vegetal.
Los aminoácidos son tan importantes para el crecimiento y desarrollo de los niños que los médicos, hasta un miligramo, han calculado el mínimo necesario, gracias al cual los hombres fuertes pueden crecer grandes y fuertes. Resultó que un niño menor de un año experimenta la mayor necesidad de lisina: 150 mg por 1 kilogramo de peso corporal, y la menor necesidad de triptófano: 17 mg. Todo esto está contenido en cantidades suficientes, por ejemplo, en platos de carne. Según los expertos, es deseable que un niño que ya tiene permitido comer carne por edad, tenga carne en su dieta diaria.
¿Ocho o diez? Generalmente se acepta que existen ocho aminoácidos esenciales: valina, isoleucina, leucina, lisina, metionina, treonina, triptófano y fenilalanina. Y esto es cierto, si estamos hablando del cuerpo formado de un adulto. Sin embargo, para los bebés, la arginina y la histidina también son indispensables. Para ayudar a memorizar los diez aminoácidos esenciales, los estudiantes de medicina usan esta divertida regla mnemotécnica: "Lisa tiró Fen en el Tribune, teniente sobria puesta en aislamiento con el guitarrista argentino".
Sin embargo, hoy en día, sin tener una granja de subsistencia propia, es bastante difícil asegurarse de que el producto destinado al niño sea de buena calidad. Por lo tanto, la carne preparada y los purés de carne y verduras de los principales fabricantes mundiales de alimentos para bebés serán la mejor opción y la más segura.
Desarrollados teniendo en cuenta las recomendaciones de pediatras y nutricionistas, se preparan a partir de productos naturales sin la adición de sal, almidón, componentes genéticamente modificados, sabores artificiales y potenciadores del sabor. La seguridad de dichos productos está garantizada tanto por la reputación del fabricante como por el control constante de numerosas autoridades de inspección.
Debido a su consistencia y combinación cuidadosa de ingredientes, platos como, por ejemplo, Heinz "Country Ternera" son fáciles de digerir y enriquecen la dieta del niño con proteínas completas, vitaminas, microelementos y ácidos orgánicos necesarios para un crecimiento exitoso. Una amplia gama de purés de carne ofrecidos por los fabricantes permitirá que la nutrición del pequeño sea lo más variada posible, presentándole periódicamente nuevos sabores interesantes, dándole un sabor a pavo tierno, carne de conejo o pollo.
¿A qué conduce un déficit? La deficiencia de aminoácidos esenciales puede tener consecuencias graves y, a veces, incluso irreversibles. Cuando una deficiencia de proteínas comienza a desarrollarse en el cuerpo de un niño, los órganos y tejidos, para los cuales la renovación intensiva es lo más importante, por ejemplo, los intestinos, sufren en primer lugar. También es posible el desarrollo de anemia, disminución de la masa del hígado, debilitamiento del sistema inmunológico y, finalmente, inhibición del crecimiento del cabello y caléndulas.
Así, introduciendo paulatinamente los complementos cárnicos en la dieta del bebé, los padres no solo le proporcionarán la mejor nutrición, sino que inculcarán al bebé el hábito de los productos naturales desde la primera infancia y, con ello, le proporcionarán un futuro saludable.
- En contacto con 0
- Google+ 0
- OK 0
- Facebook 0